| CATEGORII DOCUMENTE |
| Bulgara | Ceha slovaca | Croata | Engleza | Estona | Finlandeza | Franceza |
| Germana | Italiana | Letona | Lituaniana | Maghiara | Olandeza | Poloneza |
| Sarba | Slovena | Spaniola | Suedeza | Turca | Ucraineana |
DOCUMENTE SIMILARE |
|
ALIFATINIAI IR AROMATINIAI ANGLIAVANDENILIAI
Alkanř struktűra ir savybës
Fizikinës savybës
Angliavandeniliai, kuriems bűdinga linijinë C atomř grandinë ir s ryšiai tarp atomř, vadinami sočiaisiais angliavandeniliais, pagal sisteminę nomenklatűrą – alkanais.
Alkanř molekulës nepolinës, kadangi jas sudaro nepoliniai C-C ir C-H ryšiai. Tarp alkanř molekuliř sąveika nedidelë. C1-C4 – dujos, C5-C17 – skysčiai, C18 - … - kietos medžiagos. Alkanai yra lengvesni už H2O ir nesimaišo su juo. Tarp alkanř ir H2O molekuliř vyrauja atostűmio jëgos – hidrofobinë tarpmolekulinë sąveika, kuri yra alkanř ir H2O išsisluoksniavimo priežastis. Alkanř C atomř grandinës yra gyvosios materijos hidrofobiniř savybiř nešëjos.
Nedideliř matmenř alkanř molekulës (iki C8)
gali ásiterpti á vandens asociatř ertmes ir
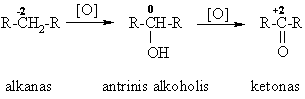
Cheminës savybës

Schemoje pateiktos reakcijos yra oksidacijos – redukcijos reakcijos, kadangi kinta C atomř oksidacijos laipsnis
Radikalinës pakeitimo reakcijos (SR)

Alkanř nitrinimas

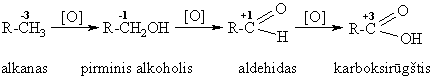
![]()
Biologinis alkanř oksidavimas
Heterolizinis oksidavimas (mitochondrijose)
alkanř dehidrogenazinis oksidavimas

monooksigenazinis oksidavimas (hidroksilinimas)
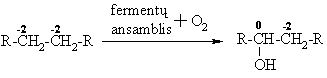
Ši reakcija yra organinio svetimkűnio, turinčio alkilř radikalř, pašalinimo iš organizmo pirmoji stadija(didina jo hidrofiliškumą).
Homolizinis (laisvaradikalinis) oksidavimas
Pagrindinis radikalř šaltinis organizme yra molekulinis O2. Dalinai redukuojant deguoná susidaro ávairios aktyviosios (toksinës) jo formos:
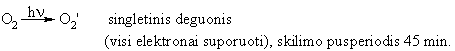


![]()
Esant radiaciniam poveikiui, aktyviosios deguonies formos organizme susidaro ir iš H2O:
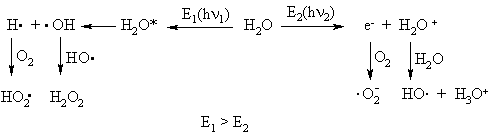
Be to, deguonies radikalai gali susidaryti iš metaloproteinř ir deguonies:


Normalaus intensyvumo laisvaradikalinis oksidavimas yra bűtinas metabolizmui.
Kai radikalř susidarymo greitis ir jř koncentracija ląstelëje viršija tam tikrą ribą, laisvaradikaliná oksidavimą lëtina organizmo daugiakomponentë antioksidacinë buferinë sistema, kuri radikalus paverčia mažai aktyviais junginiais (nutraukiama grandininë reakcija).
Šias funkcijas atlieka:
antioksidatoriniai ir antiperoksidiniai fermentai: superoksiddismutazë, katalazë, gliutationperoksidazë;
antioksidatoriai – pasižymintys redukcinëmis savybëmis organiniai junginiai: ávairűs tioliai (glutationas, cisteinas, dihidrolipo rűgštis), askorbo rűgštis (vitaminas C), b-karotinas, vitaminai E (tokoferolis), K, P ir steroidiniai hormonai.
Antioksidacinë sistemos buferinë talpa ribota. Peržengus kritinę ribą atsiranda “oksidacinis stresas”.

Alkanř izomerizacija
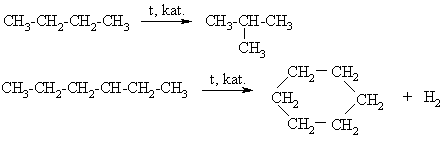
2.2. Cikloalkanř cheminiř savybiř ypatumai
Cikloalkanams kaip ir alkanams bűdinga SR. Mažieji cikloalkanai (ciklopropanas ir ciklobutanas) dël kampř átampos dar dalyvauja ir AR.
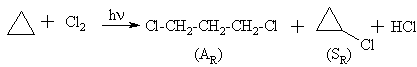
Alkanř ir cikloalkanř taikymas medicinoje:
mažos molekulinës masës alkanai taikomi vietinëje anestezijoje;
ciklopropanas – bendroje narkozëje;
tirpikliai gamtiniř medžiagř (riebalř ir eteriniř aliejř) ekstrakcijoje;
vazelino pagrindu ruošiami išoriniam naudojimui vaistai (alkanai gerai tirpsta riebaluose ir lengvai difunduoja per odą).
2.3. Alkenř struktűra ir savybës
Alkenams bűdingas dvigubasis ryšys tarp anglies atomř.
Alkenai turi daugiau struktűriniř izomerř, negu to paties anglies atomř skaičiaus alkanai, nes jř kieká lemia ne tik anglies atomř grandinës šakotumas, bet ir dvigubojo ryšio padëtis joje. Be to, alkenams bűdinga ir stereoizomerija (p-diastereomerija).
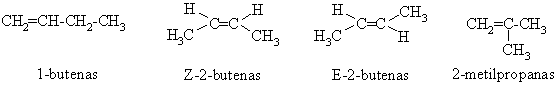
Alkenř fizikinës savybës, áskaitant ir hidrofiliškumą, panašios á alkanř. Mažos molekulinës masës alkenai gyvame organizme sukelia narkotiná efektą.
Jungimosi reakcijos

Alkenř cheminá aktyvumą lemia dvigubasis ryšys, kuris pasižymi elektronř donorinëmis savybëmis ir yra lengvai poliarizuojamas. Be to, jis daro átaką alilo padëties C-H ryšiř aktyvumui. Kadangi C=C ryšys yra nukleofilinis, jis dalyvauja elektrofilinio (AE) ir radikalinio (AR) prijungimo reakcijose. Alilo padëties C-H ryšys lengvai homoliziškai disocijuoja, todël jis dalyvauja radikalinio pakeitimo (SR) reakcijose.
Alkenř elektrofilinio jungimosi reakcijos (AE)
Hidrinimas
![]()
Hidrohalogeninimas
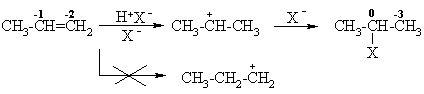
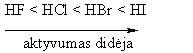
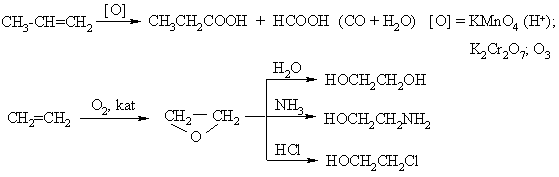
Hidratavimas

Tokia reakcija yra viena iš organizme vykstančio riebalř rűgščiř b-oksidavimo stadijř.
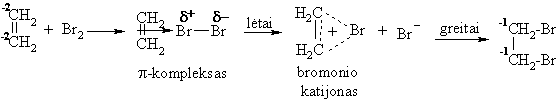
Alkenř radikalinio jungimosi reakcijos (AR)
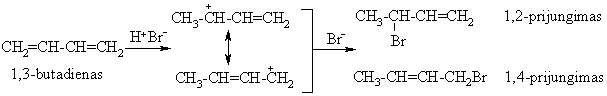
Hidrobrominimas
![]()

Šitas pavyzdys rodo, kad biocheminë jungimosi prie dvigubojo ryši reakcija gali vykti kita linkme, jei dël radiacinio švitinimo arba laisvaradikalinio oksidavimo organizme atsirastř laisvřjř radikalř.

Alkenř polimerizacija gali vykti pagal joniná (elektrofiliná-nukleofiliná) bei laisvaradikaliná mechanizmą.
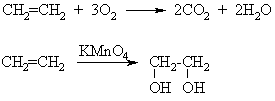
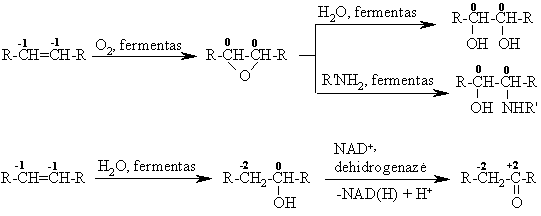
Laisvaradikalinis oksidavimas

Jei
oksiduojama atmosferos oro deguonimi – autooksidacija.
2.4. Konjuguotř dienř struktűra ir savybës
Jungimosi reakcijos
Polimerizacija
Polimerizacija gali vykti pagal joniná arba laisvaradikaliná mechanizmą.

(C5H8)2n – terpenai, izopreno (C5H8) di-, tetra- arba heksamerizacijos produktai.
Terpenai bűna neciklinës ir ciklinës (di-, tri- ir policiklinës) struktűros.

Terpenai aptinkami augaluose, spygliuočiř dervoje, kaučiukiniř augalř sultyse.
Terpentinas – terpenř mišinys.
Terpenoidai – terpenř dariniai, turintys –OH, -CHO, =C O funkcines grupes.
Terpenř grupuotës (izoprenoidinës grandinës) áeina á sudëtingř biologiškai aktyviř junginiř (vitamino A, abieto rűgšties, skvaleno, karotinoidř) sudëtá.
2.5.Aromatiniai angliavandeniliai (arenai)
Turtingi anglimi cikliniai angliavandeniliai su bűdinga jiems cikloheksatrieno ryšiř sistema ir pasižymintys ypatingomis fizikinëmis bei cheminëmis savybëmis vadinami arenais (aromatiniais angliavandeniliais).
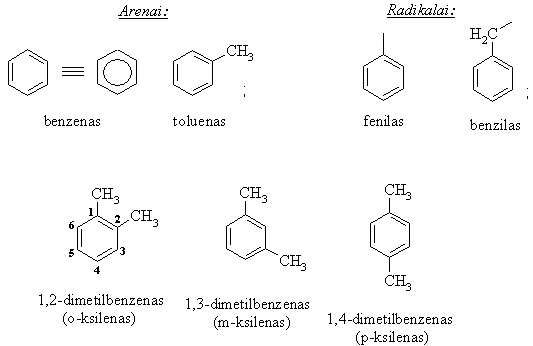
Benzeno žiedas - p elektronř donoras, todël reaguoja su elektrofilais. Benzeno p elektronř sistema sunkiai poliarizuojasi bei blogai poliarizuoja reagentą, todël aktyvinti reagentą dažnai naudojami katalizatoriai.
Elektrofilinës pakeitimo reakcijos (SE)
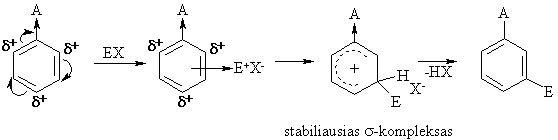
Bendrasis mechanizmas:

Pakaitř átaka
Pakaitř elektroniniai efektai veikia elektronř tankio pasiskirstymą nereaguojančioje substrato molekulëje (statinis faktorius), taip pat elektronř tankio pasiskirstymą junginyje reakcijos metu, t.y. susidarančiř tarpiniř kompleksř stabilumą (dinaminis faktorius). Reakcijai daug didesnę reikšmę turi dinaminis faktorius.
Aromatinio žiedo elektronř donoriniai pakaitai reakciją greitina, o elektronř akceptoriniai – lëtina.
Benzeno žiede elektronř donoriniai pakaitai nukreipia naują pakaitą á orto- ir parapadëtis (pirmos eilës pakaitai), o elektronř akceptoriniai – á metapadëtá (antros eilës pakaitai).
Pirmos eilës pakaitai (elektronř donorai, o- ir p-orientantai):
![]()

Pavyzdžiai:
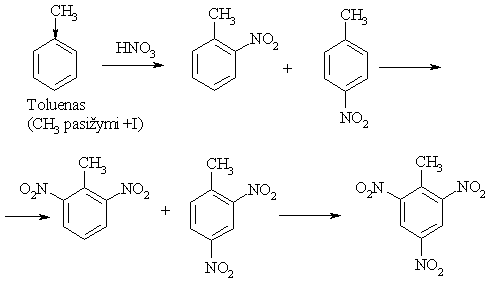
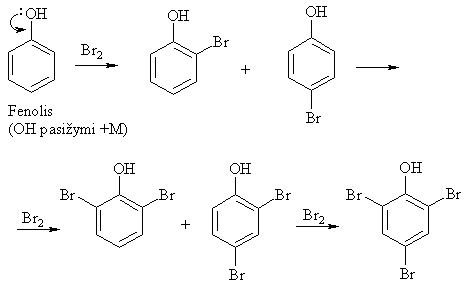
Antros eilës pakaitai (elektronř akceptoriai, m-orientantai):
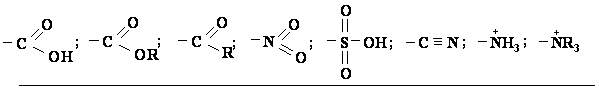
Pavyzdžiai:
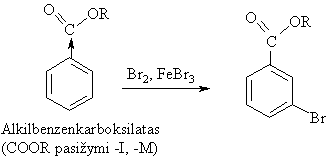

Radikalinës jungimosi reakcijos (AR)
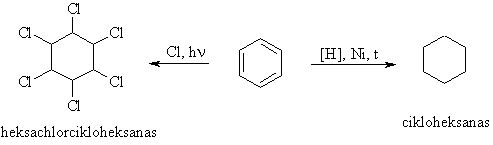

Benzeno homologams bűdingos SE ir SR reakcijos.

Organizme biocheminiř reakcijř mechanizmas gali kisti dël UV spinduliavimo, radiacijos arba perteklinio laisvaradikalinio oksidavimo.
Oksidavimas deguonimi, biologinis oksidavimas
Benzenas, skirtingai negu artimiausi homologai (toluenas, ksilenas), be galo atsparus ne tik cheminiam, bet ir biologiniam oksidavimui. Dël tos priežasties jis kaupiasi organizme, yra kumuliacinis nuodas ir labai toksiškas, ypač moterims.
Cheminio ir biologinio oksidavimo reakcijose dalyvauja su benzeno žiedu susijungę anglies atomai.
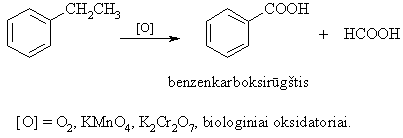
Ši benzeno homologř savybë apsprendžia mažą jř toksiškumą.
Kondensuotř arenř (naftaleno, benzpireno) cheminiř savybiř ypatumai

Gebëjimu lengvai oksiduotis aiškinamas benzpireno kancerogeniškumas.

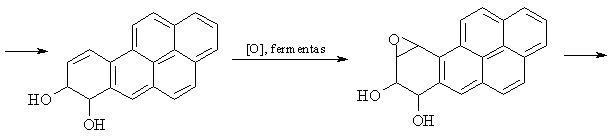
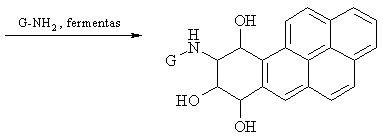
Benzpireno oksidacijos produktai, reaguodami su DNR esančio guanino aminogrupe (G-NH2), padaro DNR molekulëje negrážtamus pokyčius, skatinančius vëžiniř ląsteliř susidarymą.
Išmokę šá skyriř turite žinoti:
alkanř, alkenř ir arenř struktűrą, izomeriją, nomenklatűrą bei jiems bűdingus cheminius ryšius;
alkanř ir alkenř fizikines bei chemines savybes, jř biologinio oksidavimo ypatumus;
konjuguotř alkadienř struktűrą ir cheminiř savybiř ypatumus, mokëti apibűdinti terpenus;
arenř chemines savybes, pakaitř orientuojamąjá poveiká ir arenř biologinio oksidavimo ypatumus.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 4913
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved