| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Pile galvanice primare
1 Sisteme apoase
1.1 Pila Leclanche.Pilele primare avand o
solutie apoasa de electrolit reprezinta cele mai vechi si raspandite surse de
putere electrochimice.Prototipul lor il constituie pila prezentata inca in
1867, la expozitia de ![]() O+ pe Zn, solubilitatii extrem de reduse a
MnO
O+ pe Zn, solubilitatii extrem de reduse a
MnO![]() , a pretului de cost coborat, a usurintei
de fabricare si a unor performante ce fac pila utilizabila intr-un larg domeniu
de aplicatii practice.
, a pretului de cost coborat, a usurintei
de fabricare si a unor performante ce fac pila utilizabila intr-un larg domeniu
de aplicatii practice.

Fig.3 Pila Leclanche
In varianta clasica, pila Leclanche se poate simboliza prin urmatorul lant electrochimic:
(-) Zn/NH![]() Cl, ZnCl
Cl, ZnCl![]() /MnO
/MnO![]() , C(+)
, C(+)
In ciuda aparentelor, REMA este complexa, inca, nu total elucidata.
Procesele potential active
de baza constau in oxidarea zincului la anod si reducerea Mn![]() la Mn
la Mn![]() la catod
la catod
anod: Zn = Zn![]() + 2e
+ 2e![]()
catod: 2MnO![]() + 2H
+ 2H![]() O + 2e
O + 2e![]() = 2MnO.OH +
2OH-
= 2MnO.OH +
2OH-
sau global:
2MnO![]() + 2H
+ 2H![]() O + 2e
O + 2e![]() +Zn =
Zn(OH)
+Zn =
Zn(OH)![]() + 2MnO.OH
+ 2MnO.OH
Prezenta ZnO.Mn![]() O
O![]() , Mn
, Mn![]() O
O![]() .H
.H![]() O, ZnO,
Zn(NH
O, ZnO,
Zn(NH![]() )2Cl
)2Cl![]()
si a ZnCl![]() . 4Zn(OH)
. 4Zn(OH)![]() alaturi de
produsii de reactie mentionati in REMA globala, demonstreaza complexitatea
acesteia.
alaturi de
produsii de reactie mentionati in REMA globala, demonstreaza complexitatea
acesteia.
Componentele principale ale pilei Leclanche sunt anodul, catodul si solutia de electrolit.
Anodul,odinioara numai din zinc, azi se
confectioneaza dintr-un aliaj ternar Zn-Pb-Cd, cele din urma fiind prezente in
concentratie mica, pentru imbunatatirea proprietatilor mecanice, deseori se si
amalgameaza, pentru a minimaliza autodescarcarea.Potentialul electrodului Zn/Zn![]() depinde de
concentratia ZnCl
depinde de
concentratia ZnCl![]() , iar in
prezenta NH
, iar in
prezenta NH![]() Cl cauzeaza
deplasarea curbei spre valori mai negative, iar din cauza formarii unor
complecsi ai zincului
Cl cauzeaza
deplasarea curbei spre valori mai negative, iar din cauza formarii unor
complecsi ai zincului
Principala cauza a polarizarii anodice o
constituie acumularea ZnCl![]() (si a altor
saruri complexe de Zn), in zona perianodica.Daca livrarea energiei electrice se
intrerupe, se creeaza conditii pentru transferul de masa al acestor compusi
spre volumul solutiei de electrolit, polarizarea este micsorata si tensiunea la
borne refacuta.
(si a altor
saruri complexe de Zn), in zona perianodica.Daca livrarea energiei electrice se
intrerupe, se creeaza conditii pentru transferul de masa al acestor compusi
spre volumul solutiei de electrolit, polarizarea este micsorata si tensiunea la
borne refacuta.
Catodul este MnO![]() , in ultima
vreme, in principal, de provenienta electrolitica, fara proprietati
electronice, conductoare si cu o buna suprafata specifica.In tara noastra, la
Baia Mare, prepararea electrolitica a MnO
, in ultima
vreme, in principal, de provenienta electrolitica, fara proprietati
electronice, conductoare si cu o buna suprafata specifica.In tara noastra, la
Baia Mare, prepararea electrolitica a MnO![]() prin
oxidare anodica are la baza electrolizaunei solutii de MnSO
prin
oxidare anodica are la baza electrolizaunei solutii de MnSO![]() .Pentru
imbunatatirea conductiei electronice, MnO
.Pentru
imbunatatirea conductiei electronice, MnO![]() se amesteca
intim cu negru de fum (negru de acetilena) sau grafit.
se amesteca
intim cu negru de fum (negru de acetilena) sau grafit.
Lucrari recente demonstreaza ca reactia de
depolarizare a MnO![]() decurge in
doua trepte: cea dintai constituind un sistem redox monofazic solid, iar cea
de-a doua o descarcare in sistem solid bifazic; initial potentialul scade;
suprapotentialul este mai mic la MnO
decurge in
doua trepte: cea dintai constituind un sistem redox monofazic solid, iar cea
de-a doua o descarcare in sistem solid bifazic; initial potentialul scade;
suprapotentialul este mai mic la MnO![]() electrolitic.
electrolitic.
Electrolitul initial al pilei era o solutie
apoasa, saturata, de NH![]() Cl, dar
numai dupa vreo douazeci de ani, alaturi de NH
Cl, dar
numai dupa vreo douazeci de ani, alaturi de NH![]() Cl, s-a
adaugat ZnCl
Cl, s-a
adaugat ZnCl![]() .Utilizarea ZnCl
.Utilizarea ZnCl![]() diminueaza
scurgerea din pila.Formarea fazelor solide are loc in timpul functionarii si se
soldeaza cu modificari ale pH-ului si rezistivitatii electrolitului, ambele
avand efecte negative asupra functionarii
diminueaza
scurgerea din pila.Formarea fazelor solide are loc in timpul functionarii si se
soldeaza cu modificari ale pH-ului si rezistivitatii electrolitului, ambele
avand efecte negative asupra functionarii
Tipuri de pile Leclanche si
caracteristicile lor.Pilele
Leclanche se fabrica intr-o gama constructiva larga si caracteristici bine
diversificate.Formele sunt cilindrica,plata si paralelipipedica, iar gabaritele
celor dintai oscileaza intre diametrul de
Tipul cilindric se construieste si intr-o alternativa in care anodul de zinc, construit din placi asezate central in forma de aripi, este inconjurat de electrolit si de masa catodica.Deoarece zincul nu serveste ca recipient, scurgerile sunt minimizate; preluarea potentialului masei catodice se realizeaza cu ajutorul unui strat subtire de metal, aflat in contact cu acesta.
Tehnica de fotografiere
'polaroid' a stimulat aparitia unei noi variante de baterie plana,
echipata cu electrozi bipolari; compania japoneza Matsushita comercializeaza
pile numite 'paper battery', extraplate, avand diverse forme si masa
de ordinul gramului.De exemplu pila discoidala avand diametrul de
Caracteristicile de functionare sunt conditionate constructiv si de regimul de exploatare .La tip constructiv identic si sarcina data, viata pilei depinde de gabarite: cu cat acestea sunt mai mari, functionarea este mai indelungata.La o pila data durata de functionare variaza invers cu viteza de descarcare.Temperatura are un efect pozitiv asupra vitezei de generare a energiei, dar scurteaza viata pilei.Un efect negativ al temperaturii se poate mentiona in legatura cu depozitarea: cu cat temperatura e mai coborata, pierderile prin autodescarcare sunt mai mici.
Performantele superioare ale pilei Leclanche alcaline se datoreaza si unor modificari de executie a componentelor esentiale.Pilele Leclanche alcaline depasesc pilele Leclanche standard printr-o rezistenta interna mai mica, prezinta o curba de descarcare mai plata si functioneaza in bune conditii, intr-un domeniu termic mai lung.De asemenea se poate mentiona o autodescarcare mai redusa.
Pile tip Leclanche, avand anod de magneziu sau aluminiu.Inlocuirea zincului cu aluminiu sau cu magneziu se justifica prin capacitatile specifice masice net superioare: aluminiu de 63 ori iar magneziul de 2.68 ori mai mare decat a zincului si prin potentiale de electrod mult mai negative, ceea ce ar permite, la mase egale, livrarea unor cantitati de energie de aproape 5 ori mai mari.In realitate, din cauza coroziunii, aceste metale se acopera cu un strat de oxid, potentialul de electrod fiind unul mixt exterior ceea ce face ca energia livrata pe uniatatea masica sa fie la magneziu de numai
2,5 ori mai mare.Tensiunea la borne este de 1,9V, mai mare cu 0,3-0,4V decat la pila Leclanche standard, iar caracteristica de descarcare superioara acesteia din urma.
Pila Mg/MnO2 se fabrica anual in zeci
de milioane de exemplare,in varianta R20 (cu destinatie specifica) si varianta
cilindrica neclasificata, avand diametrul de
Anodul de aluminiu se bucura de o masa echivalenta de ~9g, favorabila, doar cu putin mai mare ca a litiului (~7g/echivalent). Capacitatea specifica masica este superioara magneziului, iar capacitatea volumica depaseste de 2,1 ori pe cea a magneziului si de 1,4 ori pe cea a zincului.Apoi, aluminiul este un element abundent in scoarta terestra, iar Al(OH)3, produs al REMA, poseda proprietati amfotere, ceea ce permite functionarea pilei intr-un domeniu foarte larg de pH.
Desi oxidul superficial, pasivat, confera aluminiului in medii neutre sau acide un potential de electrod catodic mixt, totusi pila Al/MnO2, construita ca pila Mg/MnO2, este competitiva, gratie masei echivalente a aluminiului.Pilele echipate cu Al,desi superioare electrochimic celor cu anod de zinc, sunt mai scumpe de vreo doua ori, iar dezavantajele, cauzate de pasivare,nu sunt recomandate pentru viitor, decat in medii neapoase.
1.2 Pile primare activate inainte de utilizare.Uneori, pila primara, echipata cu anod de Mg, Zn, mai rar Pb, avand diverse mase de depolarizant catodic se activeaza numai in momentul utilizarii, prin adaos de apa, de electrolit special preparat sau numai de gaz.Asemenea pile se pot depozita in stare uscata 'inactiva' ani de-a randul, punerea in contact a cuplului electrochimic cu electrolitul facandu-se prin simpla imersie sau printr-un mecanism cu declansare automata.
Primele doua sisteme sunt mai importante, si de exemplu in cazul celui dintai, reprezentat prin lantul electrochimic:
Mg/apa de mare/AgCl
Forta electromotoare este cuprinsa intre 1,7 si 1,9V, valori departate de cea calculata.Densitatile de energie masice cifreaza la ~100Wh/kg, iar curentul se debiteaza intr-un larg domeniu de timp: de la cateva secunde, la cateva ore sau chiar cateva zile.Evolutia curbei de descarcare difera fata de mersul curbelor de descarcare standard, care marcheaza o scadere a tensiunii la bornele pilei, deoarece se manifesta simultan doua contributii diferite in sistem: depasirea timpului mort datorat strapungerii stratului pasivat de pe anodul de magneziu si scaderea rezistentei ohmice a solutiei de electrolit, gratie aparitiei si concentrarii MgCl2 in acesta.
Bateriile mari, insumand tensiuni la borne de cateva sute de volti, se utilizeaza pentru scopuri speciale marine, iar pilele mai mici, de cativa volti, fac parte din sisteme de semnalizare mare-aer ale jachetelor si ale barcilor de salvare.
.Pentru a obtine pile cu densitati
volumice de energie superioare,depolarizantul conventional MnO![]() , s-a
inlocuit, cu oxizi de metale mai grele decat manganul (Ni, Cu, Ag, Hg).Forma
constructiva este cilindrica de preferinta miniaturizata (buton), iar unele cum
ar fi, de exemplu, pila Zn/HgO, se cunosc din secolul trecut dar nu au primit
solutie tehnologica decat acum vreo 40 ani.Avand inaltime de sub 5mm si
diametrul depasind cu putin 10mm, productia lor avand un progres exploziv.
, s-a
inlocuit, cu oxizi de metale mai grele decat manganul (Ni, Cu, Ag, Hg).Forma
constructiva este cilindrica de preferinta miniaturizata (buton), iar unele cum
ar fi, de exemplu, pila Zn/HgO, se cunosc din secolul trecut dar nu au primit
solutie tehnologica decat acum vreo 40 ani.Avand inaltime de sub 5mm si
diametrul depasind cu putin 10mm, productia lor avand un progres exploziv.
1.Pila Zn/HgO, purtand si numele
Ruben-Mallory a aparut in deceniul al 5-lea al secolului nostru, are la
baza anod de Zn amalgamat, solutie apoasa concentrata de KOH (40%), saturata cu
ZnO si ca polarizant catodic amestec de HgO+grafit.Anodul si catodul se
construiesc prin presarea pulberii de zinc si respectiv HgO+grafit,
colectoarele de curent fiind constituite de corpul butonului si capacul, izolat
cu o garnitura de masa plastica de corp.Masa catodica se dimensioneaza in exces
fata de masa anodului, iar stratul de polimer microporos evita scurtcircuitul
pe care l-ar provoca mercurul metalic rezultat.Capacitatea specifica a pilei
atinge 400Ah/dm![]() , iar densitatea de energie volumica
este de 4-5 ori mai mare decat a pilei Leclanche standard; autodescarcare
minima si o functionare mai greoaie la temperaturi coborate.Pila se construieste
si intr-o alternativa secundara, regenerabila.
, iar densitatea de energie volumica
este de 4-5 ori mai mare decat a pilei Leclanche standard; autodescarcare
minima si o functionare mai greoaie la temperaturi coborate.Pila se construieste
si intr-o alternativa secundara, regenerabila.
1.4 Pila Zn/Ag![]() O depaseste
performantele pilei cu depolarizant catodic de HgO si este mai scumpa.Solutia
de electrolit (KOH sau NaOH) este decisa de destinatia pilei; cel dintai se
gaseste in pila ce alimenteaza ceasuri electrice echipate cu diode emitatoare
de lumina sau prevazute cu sistem de iluminare si alarmare, pe cand solutia de
NaOH, avand rezistenta ohmica mai mare, se gaseste in pile ce alimenteaza
ceasuri echipate cu dioade cu cristal lichid.
O depaseste
performantele pilei cu depolarizant catodic de HgO si este mai scumpa.Solutia
de electrolit (KOH sau NaOH) este decisa de destinatia pilei; cel dintai se
gaseste in pila ce alimenteaza ceasuri electrice echipate cu diode emitatoare
de lumina sau prevazute cu sistem de iluminare si alarmare, pe cand solutia de
NaOH, avand rezistenta ohmica mai mare, se gaseste in pile ce alimenteaza
ceasuri echipate cu dioade cu cristal lichid.
Acest tip de pila se construieste si intr-o versiune mare, prin asamblare in serie, pentru obtinerea unor tensiuni si capacitati mari.Si pila Zn/AgO se construieste in varianta secundara
Introducerea oxidului AgO in amestecul
catodic, alaturi de Ag![]() O
imbunatateste cu 20% capacitatea pilei, in comparatie cu pila ce contine numai
Ag
O
imbunatateste cu 20% capacitatea pilei, in comparatie cu pila ce contine numai
Ag![]() O; oxidul
superior AgO nu se poate utiliza singur, fiind nestabil si descompunandu-se cu
degajare de oxigen.
O; oxidul
superior AgO nu se poate utiliza singur, fiind nestabil si descompunandu-se cu
degajare de oxigen.
1.5Pila Mg/oxizi de
metale Anodul de magneziu a fost asociat si cu
alti oxizi decat MnO![]() , in
prezenta solutiei apoase de Mg(ClO
, in
prezenta solutiei apoase de Mg(ClO![]() )
)![]() ca
electrolit.Unele sisteme se preconizeaza utilizate in varianta activata, din
cauza vietii scurte in prezenta electrolitului.Se pare ca unele dezavantaje ale
acestor sisteme nu pledeaza pentru inlocuirea MnO
ca
electrolit.Unele sisteme se preconizeaza utilizate in varianta activata, din
cauza vietii scurte in prezenta electrolitului.Se pare ca unele dezavantaje ale
acestor sisteme nu pledeaza pentru inlocuirea MnO![]() .O mentiune
speciala merita depolarizantul organic (m-dinitrobenzen) a carui reactie
potential activa implica 12e-.Capacitatea masica este de ~2Ah/g.La temperatura
ordinara cuplul Mg/mDNB manifesta stabilitate, palierul de descarcare fiind
orizontal timp indelungat, capacitatea compensand tensiunea la borne relativ
mica (~1,1V).Din pacate, la regim termic situat mult sub temperatura ordinara,
performantele sunt mult mai mici, din cauza reducerii capacitatii.
.O mentiune
speciala merita depolarizantul organic (m-dinitrobenzen) a carui reactie
potential activa implica 12e-.Capacitatea masica este de ~2Ah/g.La temperatura
ordinara cuplul Mg/mDNB manifesta stabilitate, palierul de descarcare fiind
orizontal timp indelungat, capacitatea compensand tensiunea la borne relativ
mica (~1,1V).Din pacate, la regim termic situat mult sub temperatura ordinara,
performantele sunt mult mai mici, din cauza reducerii capacitatii.
1.6 Pile primare hibride.Sisteme metal/aer.Sisteme hibride, intrunind un anod metalic prezent in
pilele de tip Leclanche si un electrod de oxigen diluat (aer) propriu pilei de combustie se realizeaza in varianta
primara si secundara.Datorita starii gazoase, oxigenul catodic se
caracterizeaza printr-o masa mica si deci o foarte mare capacitate
masica.Prototipul il constituie sistemul Zn/aer si in varianta constructiva
cilindrica R20, poseda dublul densitatii de energie masice a pilei Zn/HgO si
inzecitul densitatii pilei Leclanche standard, atunci cand se descarca cu o
intensitate de curent mijlocie (250mA). Variantele constructive mari intrunesc
densitati de energie masice de ~200Wh/kg si capacitati de pana la 150Ah/dm![]()
Fiind caracterizata printr-o densitate de curent foarte mica, reactia de activare a oxigenului detine controlul cinetic si de aceea electrodul de oxigen se realizeaza astfel incat sa ofere o suprafata de reactie cat mai mare.
Electrolitul este NaOH, care se dizolva in apa, iar reactiile potential active constau in oxidarea zincului la zincat/oxid de zinc si reducerea oxigenului:
Zn + 4OH![]() = ZnO
= ZnO![]() + 2H
+ 2H![]() O + 2e-
O + 2e-
1/2O![]() + H
+ H![]() O + 2e- =
2OH
O + 2e- =
2OH![]()
Oxidul de zinc precipita atunci cand se depaseste produsul de solubilitate al zincatului.
Din metalele care s-au recomandat ca anozi (Zn, Mg, Al, Li) doar cel dintai s-a validat, deoarece urmatoarele manifesta autodescarcare foarte puternica din cauza coroziunii; acestea se concep numai in variante care se activeaza inainte de utilizare.
Astazi anozii pilelor Zn/aer se functioneaza din pulbere de zinc presata pe colectori de curent de alama.Gratie suprafetei de reactie mari, aparitia ZnO nu dauneaza bunei functionari a electrodului in masura in care se constata la electrozii placa.
Lantul electrochimic al pilei este:
(-) Zn/NaOH/C, O![]() (aer) (+)
(aer) (+)
Pila zinc/aer si o replica a ei, magneziu/aer, se fabrica si in variante activate cu apa sau apa de mare; anodul se poate regenera pe cale mecanica.
In locul electrolitului apos de
NaOH, pila Zn/aer este comercializata si cu solutie apoasa de NH![]() Cl;
performantele sunt similare pentru cele doua cazuri.
Cl;
performantele sunt similare pentru cele doua cazuri.
Caracteristici experimentale ale unor pile primare
|
Pila |
Reactia |
Tensiunea la borne(V) |
Densitate de energie |
Pretul/kWh |
|
|
Masica (Wh/kg) |
Volumica (Wh/l) |
||||
|
Leclanche Leclanche alcalina Cu oxid mercuric Cu oxid de argint |
Zn+2MnO Zn+AgO | ||||
Tab 2.Preturi relative ale unor pile ,considerand ca etalon pila Leclanche normala.
Pretul de cost relativ ridicat(v. tab. 2) si fabricarea mai dificila fac pila Leclanche preferata in comparatie cu pila Zn-HgO si limiteaza aplicatiile acesteia din urma .Ele se intrebuinteaza acolo unde exista limitari de spatiu , in special in aparatele de ascultat folosite in corectarea surzeniei si la stimularea muschilor inimii la cardiaci.
O densitate de energie si mai mare se
obtine in pilele in care polul pozitiv este roainlocuit cu oxid de argint ( v.
tab.1) ; pretul ridicat limiteaza
utilizarea lor la cazuri speciale. Masa activa a polului pozitiv se poate
confectiona fie din Ag![]() O fie din AgO, dar din cauza solubilitatii
considerabile a amandurora, realizarea unor separatori eficienti este foarte
dificila .Cu AgO se obtine tensiunea la
borne superioara , dar potentialul sau de electrod este atat de ridicat incat
poate descompune apa cu degajare de oxigen (v.fig.4) Fig
.4 Dependenta unor potentiale de
electrod de PH
O fie din AgO, dar din cauza solubilitatii
considerabile a amandurora, realizarea unor separatori eficienti este foarte
dificila .Cu AgO se obtine tensiunea la
borne superioara , dar potentialul sau de electrod este atat de ridicat incat
poate descompune apa cu degajare de oxigen (v.fig.4) Fig
.4 Dependenta unor potentiale de
electrod de PH 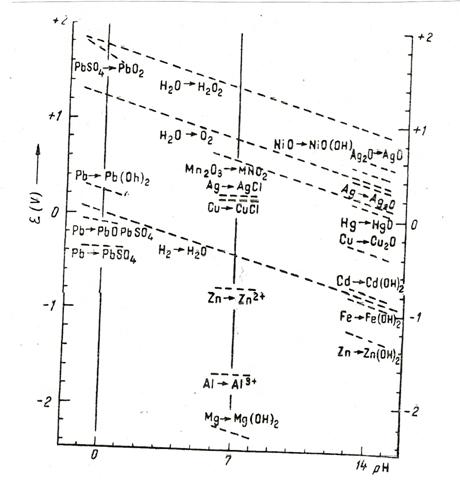
2Ag+2OH![]() àAg
àAg![]() O+H
O+H![]() O+e
O+e![]()
![]() =+0,345V
=+0,345V
2OH![]() à O
à O![]() + H
+ H![]() O+2e
O+2e![]()
![]() =+0,401V
=+0,401V
Ag![]() O+ 2OH
O+ 2OH![]() à2 AgO+ H
à2 AgO+ H![]() O +2e
O +2e![]()
![]() =+0,607V
=+0,607V
De aceea AgO se utilizeaza numai in acele pile in care electrolitul se adauga putin timp inainte de legarea lor in circuit.
In tabelul 2. figureaza tensiunile la bornele pilelor mentionate mai sus , alaturi de densitatile de
energie -masice si volumice ;in ultima coloana se compara preturile de cost
luand ca etalon pretul pilei Leclanche cu NH![]() Cl.
Cl.
Desi pretul energiei electrice produse de pilele primare depaseste cu
mai bine de 10![]() ori pretul celei obtinute de la retea, pilele primare si in special pilele Leclanche prezinta o mare importanta economica .Ea provine din
simplitatea manipularii si usurintei transportului lor.Volumul pilelor aflate in uz variaza intre 0,1 cm
ori pretul celei obtinute de la retea, pilele primare si in special pilele Leclanche prezinta o mare importanta economica .Ea provine din
simplitatea manipularii si usurintei transportului lor.Volumul pilelor aflate in uz variaza intre 0,1 cm![]() si 1 m
si 1 m![]() , ceea ce corespunde la capacitate
disponibile variind intre ordinal mAh si al 10
, ceea ce corespunde la capacitate
disponibile variind intre ordinal mAh si al 10![]() Ah si la puteri cuprinse intre cativa
Ah si la puteri cuprinse intre cativa ![]() W si catva MW.Aria utilizarii lor este extreme de intinsa, acoperind
domenii extreme de diferite , cum sunt actionarea jucariilor , alimentarea
aparatelor radio si televiziune ,aparatelor
de uz menajer ,a ceasurilor a instalatiilor de semnalizare sau chiar generarea
de energie electrica in rachete.O aplicatie remarcabila gasesc micile pile
Leclanche la stimularea batailor inimii .In ultima vreme pilele cu oxid de
mercur sunt preferate pilelor Leclanche. Ele alimenteaza un vibrator tranzistorizat , capabil sa genereze intr-un
minut circa 80 de impulsuri de 6 V si cativa mA si durate de 2 ms .Stimulatorul
se introduce prin operatie in abdomen si se inlocuieste dupa 1 sau 2 ani .
W si catva MW.Aria utilizarii lor este extreme de intinsa, acoperind
domenii extreme de diferite , cum sunt actionarea jucariilor , alimentarea
aparatelor radio si televiziune ,aparatelor
de uz menajer ,a ceasurilor a instalatiilor de semnalizare sau chiar generarea
de energie electrica in rachete.O aplicatie remarcabila gasesc micile pile
Leclanche la stimularea batailor inimii .In ultima vreme pilele cu oxid de
mercur sunt preferate pilelor Leclanche. Ele alimenteaza un vibrator tranzistorizat , capabil sa genereze intr-un
minut circa 80 de impulsuri de 6 V si cativa mA si durate de 2 ms .Stimulatorul
se introduce prin operatie in abdomen si se inlocuieste dupa 1 sau 2 ani .
2Sisteme neapoase
Pile cu anod de litiu si solventi organici.Progresul tehnologic, criza de energie, controlul asupra mediului ambiant si alte aspecte ale revolutiei tehno-stiintifice au introdus in centrul preocuparilor noi surse electrochimice de energie.Printre sisteme primare, retin atentia pilele echipate cu anod de litiu.Metal alcalin, litiul este caracterizat printr-un potential de electrod situat la minima negativa (-3,045 V/EHN), o masa echivalenta minima (~7g), capacitate specifica masica (3,86Ah/g)si volumica (7,23Ah/cm3) apreciabile, ceea ce justifica preferinta manifestata fata de el.Din cauza potentialului de electrod extrem de negativ, pilele cu litiu sunt incompatibile cu apa si, pentru dizolvarea electrolitului, se recurge la solventi organici; mai rar se utilizeaza electroliti solizi sau topituri alcaline.Utilizarea solventilor organici, care au temperaturi de solidificare inferioare apei, extind domeniul de utilizare la temperaturi scazute, unde functionarea pilele cu solutii apoase de electrolit nu este posibila.Proprietatile litiului favorizeaza pilele din punct de vedere al densitatii masice de energie, dar rezistentele interne mai mari decat ale pilelor in solutii apoase, reduc densitatile masice de putere.
Pilele primare cu anod de litiu se contruiesc, in majoritate in variante miniaturizate, fiind destinate unor consumatoare electronice de mica putere, mult mai rar in variante de putere mare.
Ele se pot clasifica, de exemplu, in functie de starea electrolitului utilizat (solutie, solvent aprotic, topitura sau solid) sau luand in considerare depolarizantul catodic: solid, lichid sau solubil in solutia de electrolit.
Solutia de electrolit(sistemul solvent + electrolit).Deoarece litiul se caracterizeaza printr-un potential de electrod situat in extrema negativa,utilizarae apei ca solvent al electrodului este exclusa.De altfel,ideea utilizarii litiuluica anod intr-o pila, chiar daca ar fi existat inainte, nu s-ar fi putut bucura de validare experimentala pana la descoperirea solventului adecvat.Aceasta se intampla in 1958, cand Harris mentioneaza stabilitatea Li in esteri ciclici, cum sunt carbonatii de propilena, de etilena si butirlactona.Tot dupa acesta data se constata si solubilitatea unor saruri de litiu in acesti solventi, cu formarea unor solutii avand conductivitati rezonabile.
Cel mai inert solvent fata de litiu este carbonatul de propilena,ii urmeaza -butirlactona si dimetilsulfoxidul.
In ceea ce priveste electrolitul, alegerea este limitata la unele saruri anorganice a caror solubilitate este acceptata de solventii aprotici.Se utilizeaza saruri simple cum sunt LiClO4 sau complexe rezultate din combinarea unei halogenuri de litiu cu un compus avand proprietati de acid Lewis: LiBF4, LiAlCl4 si LiAsF6.S-a gasit ca proprietatile conductoare ale solutiilor de electroliti mentionati, in solventi aprotici, poate fi imbunatatita prin adaos de agenti de sechestrare tip coroana gratie inhibarii fenomenului de asociere a ionilor, prin protejarea ionului de Li+ de catre campul stabilizator al atomilor de oxigen.
Amestecurile de solventi si sarurile
complexe sunt preferate in pilele secundare, din cauza unor solubilitati, si in
generala unor conductante bune.Este vrednic de mentionat ca solutia de LiAsF![]() in formiat
de metil este una dintre cela mai conductoare solutii in solvent organic, dar
utilizarea ei necesita o sare complexa de amoniu (CH
in formiat
de metil este una dintre cela mai conductoare solutii in solvent organic, dar
utilizarea ei necesita o sare complexa de amoniu (CH![]() )
)![]() NBF
NBF![]() si ca
LiAlCl
si ca
LiAlCl![]() constituie
electrolitul preferat la pilele depolarizate cu SOCl
constituie
electrolitul preferat la pilele depolarizate cu SOCl![]() si SO
si SO![]() Cl
Cl![]() .
.
Desi termodinamic nestabili,solventii utilizati in pilele cu anod de Li devin indiferenti din cauza unui strat protector format pe suprafata Li; stratul este bariera cinetica si explica autodescarcarea neglijabila a acestor pile.Urmele de apa trebuie indepartate, fie prin preelectroliza pe electrozi de platina sau prin contactul de cateza zile cu site moleculare, urmat de distilare fractionata.Stabilitatea solutiei de electrolit fata de litiu se defineste prin limita anodica a domeniului electrochimic.Ea depinde, pe langa ansamblul de solvent-electrolit, de natura metalului electrodic si de densitatea de curent.
Depolarizanti catodici din pilele primare cu anod de litiu.Principii constructive ale pilelor.Compatibilitatea catodului din pilele cu anod de litiuse exprima printr-o serie de proprietati specifice starii de agregare.Astfel, la materialele pozitive solide, insolubilitatea in solutia de electrolit reprezinta proprietatea esentiala.Dimpotriva la depolarizantii lichizi sau gazosi, solubili in solutia de electrolit, trebuie satisfacuta cerinta contrara.In rest indiferent de starea de agregare, se cer: capacitate specifica si densitate de energie mari, stabilitate chimica fata de electrolit, densitate de putere mare si o buna conductanta electronica.
Nu trebuie ignorat efectul oxidant al
unor depolarizanti (PbO![]() , MnO
, MnO![]() ) asupra
unor solventi facand parte din clasele aldehidelor si a alcoolilor sau asupra
unor solutii.Se recomanda precautii la manipularea LiClO
) asupra
unor solventi facand parte din clasele aldehidelor si a alcoolilor sau asupra
unor solutii.Se recomanda precautii la manipularea LiClO![]() , solid sau
in solutii organice, deoarece este sensibil la socuri termice sau mecanice.
, solid sau
in solutii organice, deoarece este sensibil la socuri termice sau mecanice.
Se evita separatoarele interpolare celulozice, ale caror grupe OH sunt reactive fata de Li si se prefera cele din cauciuc microporossau polipropilena.Deseori nichelul sau otelul inoxidabil si mai rar aluminiul servesc la confectionarea containerului.Depolarizantul catodic este aditionat de masa electronic conductoare, iar colectoarele de curent sunt din nichel, otel inoxidabil sau aluminiu.
Desi solutiile de electrolit realizate cu solventi organici poseda conductante net inferioare solutiilor apoase de electroliti, limitarile cinetice in functionarea pilelor provin mai degraba de la reactivitatea depolarizantului catodic decat de la transportul ionic.
Constructia anodului de litiu difera de la un tip de pila la altul, dar are la baza contactul dintre folia de litiu si banda de metal-colector de curent.Cand se urmareste realizarea unor capacitati mari, folia dreptunghiulara de litiu se ruleaza.De asemenea constructia catodului depinde de tipul si puterea pilei; o putere mare necesita o suprafata de reactie mare, obtinuta prin maruntirea fina a materialului si presarea amestecului realizat prin
amestecare cu aditivi: conductor electronic si liant.Uneori la tipurile miniaturizate liantul se poate elimina.Deseori, la pilele de mare putere, se utilizeaza separatoare interpolare.Densitati masice de energie se pot obtine cu tipul constructiv bobina.
3 Pile primare avand componentele in stare solida
Pilele galvanice construite cu electrolit solid si componente in stare solida, constituie rezultatul unor cerecetari efectuate in directia inlocuirii conductorilor ionici lichizi, avand unele dezavantaje si, in acelasi timp, in directia introducerii in circuit conversiei electrochimice a energiei, de noi materiale, posedand proprietati avantajoase din punct de vedere electrochimic sau chiar economic.Absenta unor scurgeri de lichid sau a unor emanatii gazoase, o viata lunga si un larg domeniu termic de functionare, absenta separatoarelor, posibilitatea de miniaturizare si o tehnica de fabricare simpla, constituie alte caracteristici atractive.Evident pentru a deveni avantajoasa, pila alcatuita din componente solide trebuie sa aiba o mare tensiune la borne si o joasa rezistenta interna, pentru a fi capabila de puteri si energii specifice mari
Electrolitii solizi erau cunoscuti de peste un secol, dar rezistivitatea ridicata limita utilizarea lor doar la scopuri academice.Introducerea in circuitul conversiei electrochimice a energiei, a pilelor galvanice cu componente solide se datoreaza descoperirii, spre sfarsitul deceniului al 7-lea al secolului nostru, a unor compusi avand formula generala MAg4I5, unde M=Rb, K si manifestand bune conductivitati la temperatura ordinara.Majoritatea electrolitilor solizi isi datoreaza buna conductivitate argintului (se cunosc peste 50 de asemenea electroliti), dar se cunosc si buni electroliti solizi si pe baza de cupru, sodiu, litiu, hidrogen si fluor.Electrolitii pe baza de argint au potential de descompunere apropiat de al AgI.Aceasta proprietate, precum si costul ridicat al argintului, reduc aria de utilizare a pilelor cu Ag, la aplicatii speciale.
Prezenta conductiei ionice a cristalelor solide se poate datora unor defecte de retea, localizate in nodurile retelei (defecte Schottky) sau in interstitiile ei (defecte Frenkel).In cazul celor dintai, exista o echivalenta intre defectele anionice si cele cationice,pe cand in cazul al doilea electroneutralitatea in cristal se mentine prin perechile de defect de retea-defect interstitial.Mobilitatea defectelor ionice din cristal este le baza conductiei ionice a cristalelor, explicabila prin 3 mecanisme:
-schimb intre vacanta si un ion normal al retelei cristaline;
-macanism de trecere directa a unui ion interstitial, dintr-o pozitie in alta, invecinata, echivalenta;
-mecanism indirect, de deplasare a unui ion aflat in stare normala, intr-o stare de defect interstitial, de catre un ion interstitial.
Cunoasterea mecanismului de conductie
in cristalul-electrolit solid este importanta, deoarece se poate alege metoda
de imbunatatire a transportului ionic si deci micsorarea rezistentei ohmice a
pilei.Cunoasterea mecanismului ofera posibilitatea imbunatatirii prin dopare
sau prin modificarea structurii.Mecanismul transportului poate implica anioni
sau cationi, vacante in retea sau miscare interstitiala.Determinarea numarului
de transport poate evidentia mobilitatea unor cationi mici, cum ar fi Ag+, Li+,
Na+ sau chiar a unor anioni cum sunt F- si O![]()
Electrolitul solid trebuie sa aiba o buna conductie ionica, echivalenta cu o supratensiune/polarizare ohmica minima si o conductie electronica nula, pentru a scurtcircuitarea pilei.
Pilele comercializate pentru utilizare la temperatura ordinara, sunt pe baza de anod de litiu si argint si electroliti corespunzatori.Celelalte sisteme nu au, deocamdata, decat un interes academic.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 4911
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved