| CATEGORII DOCUMENTE |
| Alimentatie nutritie | Asistenta sociala | Cosmetica frumusete | Logopedie | Retete culinare | Sport |
Intelegerea bazei genetice a variabilitatii in ceea ce priveste raspunsul la medicamentele folosite in tratarea unor afectiuni cardiace are implicatii majore nu numai in tratarea pacientilor actuali ci si pentru a ajuta la formarea unei baze pentru o mai profunda viitoare intelegere a mecanismului de actiune al medicamentelor, functie de fondul genetic al pacientului.
Insuficienta cardiaca reprezinta punctul culminant al disfunctiilor cardiovasculare, aceasta putand proveni dintr-o cardiomiopatie ischemica sau dilatativa avand la baza o boala arteriala coronariana (Cascorbi I., 2004).
In ciuda faptului ca farmacogenetica a luat amploare, rezultatele sale in cazul insuficientei cardiace sunt inca slabe. Pentru a imbunatati situatia este necesara cunoasterea modificarilor inimii la nivel molecular, structural si functional. Evidentierea unei posibile contributii genetice la evolutia bolii va permite anticiparea efectelor produse de aceasta si va ajuta la alegerea tratamentului adecvat.
Receptorii β-adrenergici au o influenta importanta asupra functiei si insuficientei cardiace. Cardiomiocitele exprima toate cele trei subtipuri de receptori: β1, β2 si β3. Subtipul β1 este cel mai des intalnit si este principalul responsabil pentru efectele cronotropice si inotropice pozitive ale catecolaminelor. Receptorul β2 determina de asemenea o intensificare a functiei cardiace, insa capacitatea sa de a semnaliza pe cai anaplerotice sugereaza o functie distincta de cea a receptorului β1.
In insuficienta cardiaca sistemul simpatic este activat iar numarul si functionalitatea β-receptorilor cardiaci sunt scazute. Numeroase studii arata alterarea sistemului β-receptorilor cardiaci. Se constata o scadere de aproximativ 50% a subtipului β1 si a ARN-ului sau mesager corelata cu o boala grava, in timp ce nivelul receptorilor β2 ramane neschimbat in cele mai multe cazuri (Juan P. Casas si colab., 2006).
Au fost descrise optsprezece variante ale receptorului
β1 si treisprezece ale receptorului β2, insa doar doua variante
genice β1 si trei β2 sunt comune. Prezenta receptorului β1 in varianta
Gly![]() (frecventa alelica 25% la populatia alba si 42% la populatia de
culoare) este asociata cu reducerea intensitatii semnalizarii cAMP dependente.
(frecventa alelica 25% la populatia alba si 42% la populatia de
culoare) este asociata cu reducerea intensitatii semnalizarii cAMP dependente.
Riscul crescut de insuficienta cardiaca la populatia de
culoare este asociat cu forma Arg![]() combinata cu receptorul α
combinata cu receptorul α![]() (frecventa alelica de 4% la populatia alba si de 38% la
populatia de culoare), care este el insusi un factor de risc (Lohse J. Martin
2003).
(frecventa alelica de 4% la populatia alba si de 38% la
populatia de culoare), care este el insusi un factor de risc (Lohse J. Martin
2003).
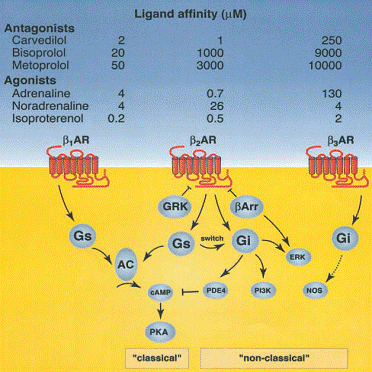
Numeroasele modificari ale sistemului β-adrenergic in insuficienta
cardiaca sunt in mare parte adaptari pentru protectia cardiomiocitelor.
Activarea agonistilor si proprietatile de cuplare ale subtipurilor receptorului β-adrenergic
(dupa Lohse J. Martin 2003 )
Hipertensiunea arteriala afecteaza 1 miliard de persoane din lumea intreaga iar bazele sale genetice sunt bine stabilite. Anual se produc 7.1 milioane de decese datorate bolilor cardiace de tipul ischemiilor si infarctelor (C. Mein si colab., 2004).
Aceasta se datoreaza efectului corelat al mai multor factori - stil de viata, dieta (aportul de sodiu), excesul de alcool, greutatea corporala.
Mecanismele moleculare ale imbolnavirilor cardiace sunt legate, in parte din cazuri, de un determinism genetic implicand forme monogenice rare ale hipo- si hipertensiunii, dar au fost facute putine progrese in identificarea genelor si mecanismelor care determina hipertensiunea in cazurile cu determinism polifactorial.
Studiile de farmacogenetica in cazul hipertensiunii au luat amploare, pentru identificarea determinismului genetic al bolii, in diferite populatii. In cursul unui studiu recent, spre exemplu, a fost evaluat raspunsul la diuretice tiazidice la 291 de persoane de origine hispanica, folosind tehnica SNP (Single Nucleotid Polymorphism). Astfel s-a constatat ca toate genele responsabile de fenotipul hipertensiv codifica produsi cu specificitate de actiune la nivelul rinichilor si care actioneaza prin afectarea nivelului de sodiu din organism (Alan Y Deng, 2007).
Warfarina este un anticoagulant recunoscut pentru actiunea sa in prevenirea bolilor tromboembolice. Terapia cu warfarina poate fi dificil de realizat si datorita variabilitatii individuale in ceea ce priveste raspunsul pacientilor. In cazul fiecarui pacient doza zilnica de warfarina variaza.
Acum este cunoscut faptul ca polimorfismul genelor care influenteaza metabolismul acestui gen de compusi (CYP2C9) si raspunsul farmacodinamic (VKOR1) sunt strans asociate cu raspunsul la warfarina.
Hemoragia severa si potential letala este singurul efect advers major asociat cu terapia cu warfarina, existenta acestui gen anume de accidente sugerand in mod evident faptul ca genotiparea ar trebui sa limiteze acest risc ( Rettie Allan, 2006).
Studiile realizate pe aproximativ 3000 de pacienti tratati cu warfarina indica faptul ca purtatorii alelelor desemnate 2 si 3 ale CYP2C9 prezinta un risc semnificativ mai crescut de hemoragie. Un alt studiu realizat pe 1000 de pacienti tratati cu acenocumarol (un analog al warfarinei) a carui metabolizare se bazeaza tot pe CYP2C9, a relevat, de asemenea, faptul ca posibilitatea producerii unei hemoragii masive este semnificativ mai mare la purtatorii alelelor desemnate 2 si 3.
Tramentul medicamentos in cazul aritmiilor cardiace a oferit o serie de date extrem de relevante pentru farmacogenetica, deoarece in cazul aritmiilor limita dintre doze si concentratii de substanta activa care induc un efect benefic si cele care induc toxicitate (inclusiv infarct) poate fi infima.
In ultimii ani s-au realizat progrese majore in intelegerea sindroamelor aritmice determinate genetic, precum sindromul QT sau sindromul Brugada.
Sindromul QT reprezinta o tulburare de ritm rara, ereditara, neinsotita de alte afectiuni, si care apare, de obicei, la copii si la adultii tineri.
Sindromul Brugada (sindromul de moarte subita) este o boala genetica caracterizata prin anomalii electrocardiografice si risc crescut de moarte subita. Pacientii pot face fibrilatie ventriculara care evolueaza rapid spre exitus, in lipsa interventiei medicale. Aproximativ 1/5 din cazuri au fost corelate cu o mutatie a genei SCN5A-3p21 care controleaza sinteza canalelor de sodiu din membrana cardiomiocitelor. Boala are transmitere autosomal dominanta si este mai frecventa la barbati. Prevalenta sa este crescuta la populatiile asiatice (Rodon M.Dan, 2000).
Progresele in intelegerea determinismului genetic nu au ajutat numai la intelegerea patogenezei in aceste sindroame, ci au oferit si un punct de pornire pentru studiile asupra modului in care variabilitatea functionala si expresia acestor gene poate influenta raspunsul la medicamente.
Medicamentele pentru care s-a demonstrat corelatia cu decesul cardiac subit includ β-blocante si inhibitori ai ACE (angyotensin converting enzyme- enzima de conversie a angiotensinei).
Polimorfismul moleculelor tinta a fost identificat pentru ambele clase. Majoritatea β-blocantelor reprezinta substrate pentru CYP2D6: metoprolol, timolol, carvedilol. Polimorfisme comune in genele pentru receptorul β2 adrenergic au fost identificate in timpul terapiei medicamentoase a astmului si la pacientii care prezinta insuficienta cardiaca (Cascorbi Ingolf si colab., 2004).
Gena pentru ACE prezinta un polimorfism al intronilor care include prezenta sau absenta [insertia (I) sau deletia (D)] unui segment de 250 de perechi de baze. Subiectii de tip DD au nivele crescute de ACE si posibil un raspuns scazut la inhibitia ACE comparativ cu subiectii cu genotip II sau ID. (Elsevier science B.V., 2001).
Trecerea medicamentelor prin membranele celulare dicteaza absorbtia, distributia, metabolizarea si excretia acestora. Acest proces este conditionat de o serie de factori care includ masa moleculara a compusilor forma lor, gradul de ionizare si proteinele legate.
Acumularea de xenobiotice in tesuturi nu depinde doar de abilitatea lor de a patrunde in celule, ci si de abilitatea de a iesi din celule. De exemplu, rolul transportorilor de eflux precum proteinele ABC (ATP-binding cassette- cutia de legare a ATP) in externalizarea compusilor medicamentosi este bine cunoscut.
Transportorii ABC actioneaza in asociere cu enzime care metabolizeaza medicamentele, pentru a proteja organismul de componentele toxice.
Cea mai studiata superfamilie de transportori sunt P-glicoproteinele. Despre acestea, s-a observat ca sunt supraexprimate in celulele tumorale, supraexprimarea lor fiind asociata cu rezistenta dobandita la medicamentele antitumorale.
P-glicoproteinele au fost evidentiate si in tesuturi normale, respectiv in ficat, rinichi, intestin si inima. Chiar daca informatiile privind rolul functional al transportorilor ABC in miocard sunt limitate, se presupune ca acestia pot modula eficacitatea si toxicitatea agentilor cardioactivi (Couture L. si colab., 2006).
La om au fost descoperiti pana acum aproximativ 50 de transportori, dintre care cel putin 14 prezinta activitate de transport al xenobioticelor.
Dovada indirecta a expresiei acestor transportori la nivelul inimii a fost obtinuta la animalele care prezinta genele transportorilor ABC. Cresterea nivelului substratelor transportorilor ABC la aceste animale a demonstrat implicarea acestor proteine in distributia medicamentelor in tesutul cardiac.
Cazurile de crestere a concentratiei medicamentelor in inima si a cardiotoxicitatii aparute in urma administrarii de substrate pentru transportorii ABC par sa confirme rolul important al acestor proteine in transportul medicamentelor catre inima.
Mecanismele toxicitatii cardiace succesive administrarii substratelor transportorilor ABC sunt complexe. Canalele ionice implicate in generarea potentialelor de actiune cardiace sunt probabil unul dintre factorii cheie indirect afectati de modularea transportorilor ABC in producerea efectelor cardiace adverse.
Polimorfismul genelor acestor transportori moduleaza receptivitatea la medicamente. Impactul lor asupra concentrarii subsatnetelor medicamentoase la nivel cardiac ramane sa fie demonstrat.(2005 Societatea Europeana de Cardiologie. Publicat in Elsevier B.V. )
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 1607
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved