| CATEGORII DOCUMENTE |
| Aeronautica | Comunicatii | Electronica electricitate | Merceologie | Tehnica mecanica |
Pile electrice si acumulatori
Cand a fost inventata bateria?
Una dintre cele mai noi si remarcabile descoperiri ale ultimilor 400 de ani a fost electricitatea.
Poate te intrebi: "Beneficiem de electricitate de atata timp?" Raspunsul este da. Dar practic,
electricitatea a inceput sa fie folosita, intr-un mod limitat, intre anii 1850-1900. De exemplu,
la expozitia internationala de la Paris din anul 1900, una dintre principalele atractii a fost un
pod peste raul Sena, luminat electric.
Cea mai veche metoda de a se genera electricitate provine din crearea unei incarcaturi statice.
In anul 1660, Otto von Guericke a construit prima masina electrica care consta dintr -un glob
mare de sulf care prin frecare si rostogolire atragea pene si bucati mici de hartie. Guericke a
fost capabil sa demonstreze ca scanteile generate erau intr-adevar electrice.
Prima idee de folosire a electricitatii statice a fost asa-zisul "pistol electric". Inventat de
Alessandro Volta (1745-1827), acesta consta intr-o bucata de sarma pusa intr-un vas umplut
cu gaz metan. Prin trimiterea unei scantei de la un capat la celalalt al sarmei vasul urma sa
explodeze.
Volta s-a gandit sa-si foloseasca inventia pentru a realiza comunicatiile la distanta, chiar
adresandu-se numai in sistem binar. Pentru aceasta, o sarma de otel sustinuta de stalpi de lemn
urma sa fie intinsa intre Como si Milan, Italia, capatul receptor al sarmei fiind introdus intr-un
vas umplut cu gaz metan. La comanda, o scanteie electrica era trimisa de-a lungul sarmei care
urma sa detoneze pistolul electric, emitandu-se astfel semnale codate. Aceasta linie de
comunicatii nu a fost construita niciodata.
In anul 1791, in timp ce lucra la Universitatea din Bologna, Luigi Galvani a descoperit ca
muschiul unei broaste se contracta cand acesta este atins cu un obiect metalic. Acest fenomen
urma sa fie cunoscut ca electricitatea animala - o utopie deoarece teoria nu a fost
demonstrata. Imboldit de aceste descoperiri, Volta a initiat o serie de experimente folosind
zinc, plumb, cositor sau otel pentru placutele incarcate cu sarcina pozitiva si cupru, argint, aur
sau grafit pentru placutele incarcate cu sarcina negativa.
Urmatoarea etapa in generarea electricitatii a fost electroliza. Volta descopera in anul 1800 ca
un flux continuu al unei forte electrice era generat cand se foloseau anumite fluide ca si
conductori pentru a produce o reactie chimica intre metale sau electrozi. Acestea au condus la
inventarea primei celule voltaice, cunoscuta sub numele de baterie. In plus, Volta descopera
ca prin suprapunerea celulelor voltaice se obtinea o crestere a tensiunii
In acelasi an, Volta si-a expus descoperirea legata de sursa continua de electricitate la
Societatea Regala din Londra. De aceasta data, experimentul nu se mai limita la o scurta serie
de scantei. De acum era disponibil curentul electric in flux continuu.
Franta a fost printre primele natiuni care a recunoscut oficial descoperirile lui Volta. In acel
moment, Franta avea acces la cele mai mari descoperiri stiintifice si ideile noi erau asteptate
cu bratele deschise pentru a sustine ordinea de zi politica. Ca urmare a invitatiilor primite,
Volta s-a adresat Institutului Francez intr-o serie de conferinte la care a fost prezent si
Napoleon Bonaparte in calitate de mebru al Institutului.
Descoperirile lui Volta au impresionat lumea in asa masura incat in noiembrie 1800 el a fost
invitat la Institutul National Francez sa tina o conferinta la care a participat si Napoleon
Bonaparte. Insusi Napoleon a ajutat la experimente, facand scantei cu bateria, topind un fir
de otel, descarcand un pistol electric si descompunand apa in elementele de baza.
S-au facut noi descoperiri cand Sir Humphry Davy, inventatorul lampii de veghe a minerului,
a instalat in subsolurile Institutului Regal din Londra cea mai mare si mai puternica baterie
electrica. El a conectat bateria la electrozii de carbune producand prima lumina electrica.
Dupa spusele martorilor, lampa cu arc voltaic a facut cel mai stralucitor arc crescator de
lumina vazut vreodata.
Cele mai importante cercetari ale lui Davy au fost dedicate electrochimiei. Dupa
experimentele lui Galvani si descoperirea celulei voltaice, interesul fata de electricitatea
galvanica devenise raspandit. Davy incepuse sa testeze efectele chimice ale electricitatii in
anul 1800. Curand a aflat ca trecand curent electric prin unele substante, aceste substante se
descompun, proces ulterior numit electroliza. Tensiunea era generata ca urmare a reactivitatii
electrolitului cu metalul. Evident, Davy a inteles ca actiunea electrolizei si a celulei voltaice
au fost la fel.
In anul 1802, Dr. William Cruickshank proiecteaza prima baterie electrica pentru productia de
serie. Cruickshank a aranjat foi patrate de arama, pe care le -a cositorit la capete cu foi de zinc
de marimi egale. Aceste foi au fost puse intr -o cutie lunga de lemn care a fost pecetluita cu
ciment. Santurile din cutie fixau placile de metal. Apoi cutia a fost umpluta cu un electrolit de
sare de mare sau apa distilata.
William Cruickshank, un chimist englez, a construit o baterie cu celule electrice prin
introducerea placilor de zinc si arama intr-o cutie de lemn plina cu electrolit. Acest proiect
avea avantajul neuscarii in timpul folosirii si furniza mai multa energie decat aranjarea cu
discuri a lui Volta.
A treia metoda de generare a electricitatii a fost descoperita relativ tarziu - electricitatea prin
magnetism. In anul 1820, AndrMarie Ampère (1775-1836) a observat ca firele purtatoare de
curent electric erau uneori atrase unul catre celalalt, alteori ele se respingeau.
In anul 1831, Michael Faraday (1791-1867) a demonstrat cum un disc de arama era capabil sa
produca un flux constant de energie cand era rotit intr-un puternic camp magnetic. Faraday,
ajutandu-l pe Davy si echipa sa de cercetare, a reusit sa genereze o forta electrica permanenta
atat timp cat miscarea intre bobina si magnet continua. A fost inventat generatorul electric.
Acest proces a fost apoi inversat si motorul electric a fost descoperit. La scurt timp, au fost
realizate transformatoarele care puteau transforma electricitatea la un voltaj dorit. In anul
1833, Faraday defineste fundamentul electrochimiei prin Legea lui Faraday, care descrie
valoarea reducerii care survine intr-o celula electrolitica.
In anul 1836, John F. Daniell, un chimist englez, continua cu studierea bateriei electrochimice
si dezvolta o celula imbunatatita care producea curent continuu, fata de echipamentul
lui Volta. Pana in acel moment, toate bateriile erau compuse din celule primare, ceea ce
insemna ca nu puteau fi reincarcate. In anul 1859, fizicianul francez Gaston Plat a inventat
prima baterie care putea fi reincarcata. Aceasta baterie se baza pe exemplul chimiei acide, un
sistem care este folosit si astazi.
Istoria dezvoltarii bateriei
1600 Gilbert (Anglia) Initierea studiilor electrochimiei
1791 Galvani (Italia) Descoperirea "electricitatii animale"
1800 Volta (Italia) Inventarea celulei voltaice
1802 Cruickshank (Anglia) Prima baterie electrica produsa in masa
1820 Ampère (Franta) Electricitatea prin magnetism
1833 Faraday (Anglia) Promulgarea Legii lui Faraday
1836 Daniell (Anglia) Inventarea celulei lui Daniell
1859 Plant (Franta) Inventarea bateriei cu acid
1868 Leclanch (Franta) Inventarea celului Lenlanch
1888 Gassner (USA) Terminarea celulei uscate
1899 Jungner(Suedia) Inventarea bateriei nichel-cadmiu
1901 Edison (USA) Inventarea bateriei nichel-otel
1947 Neumann (Franta) Recunoasterea bateriei nichel-cadmiu
Mijl. 1960 Uniunea Carbide (USA) Dezvoltarea bateriei alcaline primare
Mijl. 1970 Dezvoltarea valvei la bateria cu acid
1990 Comercializarea bateriei nichel-metal
hidrid
1992 Kordesch (Canada) Comercializarea bateriei alcaline
reutilizabile
1999 Comercializarea bateriei litiu-ion/polimer
2001 Producerea in masa a celulelor cu schimb
de protoni
Se poate ca bateria sa fi fost descoperita cu mult timp in urma. Se crede ca persii care
mergeau spre Bagdad (cca. 250 ien) foloseau baterii cu argint galvanizat. Egiptenii aveau
placi de cupru de acum 4300 de ani.
In anul 1899, Waldmar Jungner din Suedia inventeaza bateria nichel-xxx, folosind nichel
pentru electrodul pozitiv si cadmiu pentru electrodul negativ. Doi ani mai tarziu, Edison
produce un model alternativ prin inlocuirea cadmiu-lui cu otel. Din cauza costurilor ridicate
comparativ cu cele uscate sau cele cu acid, aplicatiile practice ale bateriilor nichel-cadmiu si
nichel-otel erau limitate.
Spre sfarsitul anilor 1800 se construiesc generatoare uriase si transformatoare. S-au instalat
liniile de transmisie si electricitatea s-a pus la dispozitia umanitatii pentru a produce lumina
electrica, caldura si transport. La inceputul secolului XX, inventarea tubului vacumat a facut
posibila producerea semnalelor controlate, amplificarilor si sunete lor. Imediat dupa acestea a
fost inventat radioul care a facut posibila comunicarea fara fir.
De asemenea, Shlecht si Ackermann au adus, in anul 1932, noi imbunatatiri importante.
Aceste progrese s-au reflectat in curenti de amperaje mai mari si imbunatatirea longevitatii.
Omologarea bateriei nichel-cadmiu, asa cum o stim noi astazi, devine disponibila doar cand
Neumann reuseste sa finalizeze celula, in anul 1947.
Sumar
De-a lungul timpului omenirea a devenit dependenta de electricitate, un produs fara de care
dezvoltarea tehnologiei nu ar fi fost posibila. O data cu cresterea nevoii de mobilitate, oamenii
au trecut la inmagazinarea puterii portabile - in primul rand pentru aplicatii in miscare si in al
doilea rand pentru aplicatii portabile. Asa cum noi ne uitam la neindemanarea si nesiguranta
cu care primele baterii au fost concepute, la experimentele greoaie de acum 200 de ani ale
predecesorilor nostri, in acelasi mod s-ar putea uita la tehnologia de astazi descendentii nostri.

Convesia fotovoltaica
v Notiuni introductive
v Conversia fotovoltaica
v Factorii de care depinde eficienta celulelor solare
v Conversia fotovoltaica in Romania
v Perspective in producerea curentului electric prin efect fotovoltaic
a) a) Epuizarea iminenta a rezervelor de combustibil fosil traditional (carbune, petrol, gaze naturale), problema majora pentru populatie.
b) b) Ce trebuie facut, cu ce trebuie compensata epuizarea resurselor fosile ?
criza energetica la nivel mondial a stimulat pretutindeni in lume cercetarile pentru dezvoltarea si valorificarea eficienta a unor surse noi, alternative de energie.
Interes deosebit il prezinta Soarele.
Pamantul primeste de la Soare 5180 Q=5180*2,93*1014 kWh .
Puterea radiata de Soare in afara atmosferei terestre are o densitate medie de 0,1353 W/cm2 .
La nivelul solului, densitatea puterii radiate scade datorita absorbtiei si imprastierii diferitelor gaze.
c) c) Posibilitati de utilizare a energiei solare prin transformarea ei in alte forme de energie decat cea electrica:
in energie biologica
in energie mecanca
in energie termica
d) d) Calitatea unui dispozitiv de transformare a energiei solare in energie electrica se apreciaza dupa:
eficienta de conversie
pretul de cost al dispozitivului
durata lui de viata
a) a) Prezentare generala
Antoine Becquerel a descoperit posibilitatea generarii unui curent electric in circuit sub actiunea luminii (in 1839).
Frenkel (1935), Landau (1936) au dat explicatii asupra fenomenului.
Conversia radiatiei solare in energie electrica prin efectul fotovoltaic se realizeaza in celule solare
Se realizeaza direct, fara etape intermediare de transformare in caldura.
b) b) Celula solara
dispozitiv realizat cu materiale semiconductoare.
clasificarea celulelor solare:
dupa natura neomogenitatii
homojonctiune
heterojonctiune
celule cu:
- semiconductoare monocristaline
- straturi subtiri
- policristaline sau amorfe
- pe baza de Si cele cu GaAs: dau eficienta de conversie ridicata 18-25%
- CdS policristalin, Si amorf hidrogenat: au randamente mai scazute: 5-12%
c) c) Aplicatii in care intervin celule solare ca generatoare electrice
generatoare izolate de mica putere (calculatoare de buzunar, radioreceptoare portabile)
generatoare locale de putere medie (pompe de irigatii, aparate electrocasnice, vehicule electrice)
generatoare de mare putere (pentru alimentarea retelei de curent alternativ)
O celula fotovoltaica transforma doar o parte din energia radianta in energie electrica, restul se pierde ca urmare a unei serii de procese ce se petrec in timpul conversiei:
procese care intervin cand energia este sub forma de radiatie (pierderi de radiatie)
procese care intervin dupa ce energia radianta a fost transferata semiconductorului
pentru fiecare proces se poate defini cate o "eficienta partiala"
eficienta celulei rezulta ca un produs al tuturor "eficientelor partiale"
patrunderea luminii prin suprafata
absorbtia incompleta
generarea purtatorilor
pierderi de curent datorate recombinarii
pierderi de tensiune
jumatate din energia absorbita de la soare se pierde sub forma de caldura
aceasta pierdere face ca maximum de eficienta sa fie in jur de 25%.
S-au facut cercetari incepand din anii '70 avand urmatoarele obiective:
realizarea de generatoare solare cu caracter demonstrativ
realizarea unei fabricatii de serie mica de baterii solare
dezvoltarea cercetarilor in domeniul bateriilor fotovoltaice.
In 1982 I.C.P.E. a omologat primele module fotovoltaice cu celule din siliciu monocristalin produse de I.P.R.S.. S-au facut studii privind celulele fotovoltaice lichide cu electrozi semiconductori si pentru fotoelectroliza apei. Primele baterii cu celule in strat subtire au fost realizate in perioada 1980-1984.
Energia electrica produsa prin tehnologie fotovoltaica s-a afirmat ca o sursa de electricitate viabila din punct de vedere economic si nu numai.
Vanzarile mondiale de sisteme fotovoltaice au atins in 1998 150 MW, dupa un deceniu in care au crescut cu 15-20% pe an.
Ajungand la o cifra de vanzari de aproximativ 1 miliard de dolari, industria fotovoltaica a stabilit noi standarde a patruns pe noi piete si si-a demostrat viabilitatea din punct de vedere economic.
Acumulatori li-ion
Constructie:
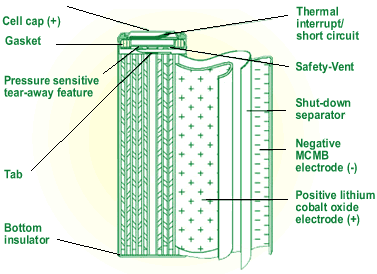
Date tehnice:
|
Model GP |
Voltaj |
Capacitate |
Dimensiune |
W (g) |
Curentul maxim de
descarcare |
Voltajul maxim de
incarcare |
Curentul maxim de
incarcare |
||
|
Tipic (mAh) |
Minimum (mAh) |
D (mm) |
H |
||||||
|
GP1767L125 | |||||||||
|
GP1850L120 | |||||||||
|
GP1850L130 | |||||||||
|
GP1865L170 | |||||||||
|
GP1865L180 | |||||||||
|
GP1865L210*1 | |||||||||
|
Acumulatori NICHEL-METAL HYDRIDE (NiMH) pentru aparatele fotografice |
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Introducere Camerele fotografice digitale din zilele noastre sunt produse electronice, dotate cu blitz, procesoare puternice, memorii de stocare, motoare electrice care actioneaza mecanismul de punere la punct, zoom-ul sau diafragma, un ecran cu LCD pentru a vedea subiectul sau fotografia captata etc., toate consumatoare de energie. Utilizarea intensiva a acestor componente epuizeaza rapid bateriile de tip Volta, chiar si pe cele 'heavy dutty'. De o perioada de timp au fost introduse in exploatare baterii de acumulatori care furnizeaza un amperaj mai mare si au marele avantaj al reincarcarii. Desi investitia initiala in baterii si in incarcator este mai mare, pe termen lung, acestea isi dovedesc rentabilitatea. Pana in urma cu circa un deceniu, bateriile cu NiCd tronau suverane in oferta de acumulatori, dar in ultimii ani au aparut si s-au extins cu repeziciune noile baterii cu Nichel-Metal-Hidrid (NiMH). In cele ce urmeaza ma voi ocupa in principal de cele mai moderne si larg raspandite pe piata baterii de acumulatori: cele cu NiMH, in formatul AA. Ele utilizeaza acelasi principiu ca cele cu NiCd, dar inlocuiesc electrodul negativ de nichel-cadmiu - responsabil de absorbtia hidrogenului - cu un aliaj (aloy) nichel-metal Acestea au trei avantaje majore: Comparatie intre bateriile disponibile pentru aparatele digitale
Electrochimie Principiul de functionare se bazeaza pe capacitatea unor aliaje
metalice de a capta (formand hidrizi) si elibera hidrogen. Pentru ca
procesele sa se desfasoare la temperatura mediului ambiant, cele mai adecvate
aliaje au fost identificate cele cu nichel si 'pamanturi rare'
(lantan, zirconiu). Aliaj+ H20 = ALIAJ(H) + OH+ 2. la polul pozitiv, se produce oxidarea hidroxidului de nichel: Ni(OH)2 + OH+ = NiOOH + H2O + e- La descarcare (in exploatare) procesele se desfasoarain sens invers,
reactiile fiind reversibile. Profilul de descarcare Principalul parametru la acumulatori este timpul de descarcare (functionare) la un anumit curent drenat de consumator. Evaluarea curenta a bateriilor este prescurtata 'C' (capacity) si este rezultatul masurarii descarcarii unei baterii noi dar bine 'conditionata', proaspat si complet incarcate. Pentru bateriile NiMH, C reprezinta curentul (in mA) pentru un timp de descarcare standard este de 5 ore, adica 0,2 C. Unii producatori folosesc curentul minim, iar altii curentul mediu; diferentele rezultate in determinarea C sunt de circa 10%
O baterie proaspat incarcata furnizeazala borne, la 20C, o tensiune de 1,4 volti. In sarcina tipica de 0,2 C - de ex 400 mA pentru una de 2000 mAh - se produce rapid o scadere a tensiunii la 1,25 V si apoi tensiunea scade incet (la 1,2 V pentru 50% C) pana la 85 % C, dupa care urmeazao scadere rapida a tensiunii la borne. Exista referenti care sustin ca si bateriile au 'memorie', adica au o curba de descarcare intrucatva influentata de precedentele cicluri de incarcare si descarcare. Experimente de laborator au arata o scadere de pana la 150 mV a tensiunii la borne si au emis teoria ca aceasta este influentata de cadmiu. Inlocuirea cadmiului in celulele cu NiMH au inlaturat aceasta problema.
Temperatura din mediul ambiant influenteazasemnificativ capacitatea de descarcare a celulelor cu NiMH; astfel, intre 10 si 40C, bateria furnizeazapeste 95% din capacitate; in schimb, la 0C capacitatea scade la 80% si ajunge doarala 20% la - 10C; vestea buna este ca, readuse la temperaturi pozitive, bateriile isi recapata complet capacitatea la care au fost incarcate. Acest fapt se explica prin scaderea vitezei de reactie la temperaturi joase. Spre deosebire de elementele galvanice, bateriile NiMH pot furniza tensiuni nominale chiar si la descarcari in circuite mari consumatoare de curent; capacitatea actuala se mentine peste 85% pana la 4*C, adica peste 1,05 V la 6 A pentru elemente de 1500 mAh.
Continuarea pastrarii in sarcina dupa descarcare completa a componentei pozitive, produce o inversare a polaritatii, prin descarcarea componentei negative (prevazuta de producator cu o capacitate mult mai mare). In continuare, se produce inversarea polaritatii si la electrodul negativ, cu inversarea tensiunii furnizate de element, producerea abundenta de hidrogen, degradarea ireversibila a electrozilor si cresterea substantiala a presiunii din celula; presiunea ridicata deschide valva de etansare si se elimina astfel pericolul exploziei. Data fiind capacitatea electrodului negativ de a capta cantitati foarte mari de hidrogen, bateriile cu NiMH sunt mai 'rezistente' la supradescarcare decat cele cu NiCd. Pentru majoritatea consumatorilor care utilizeazaelemente cu NiMH, cel mai bun indicator al opririi descarcarii este atingerea la borne a tensiunii de 0,9 V care corespunde la o descarcare de 75%; pentru consumatorii care solicita peste 1 C, atingerea tensiunii de 0,9 V la borne se produce prematur, astfel incat in baterie ramane o cantitate mare de energie restanta, cu atat mai mare cu cat se solicita multiplii de C. Folosirea tensiunii de 0,9 V este dictata de prevenirea degradarii ireversibile a bateriilor NiMH. Este posibil ca unii consumatori sa-si inceteze functionarea cu mult inainte de aceasta valoare! Majoritatea consumatorilor necesita insa baterii de celule, pentru atinge tensiunea necesara bunei functionari. Utilizarea criteriului - O,9 V * numarul de celule - ca semnal al opririi descarcarii poate duce la inversarea polaritatii si potentiala distrugere a celui mai slab element din baterie. De aceea producatorii recomanda pentru baterii de elemente folosirea formulei: TOD= [(T50%-150mV)(n-1)]-200mV Unde: TOD = tensiunea de oprire a descarcarii Incarcarea celulelor NiMH Incarcarea corecta a bateriilor cu NiMH este esentiala pentru conservarea caracteristicilor si o utilizare indelungata. Incarcarea trebuie facuta cat mai rapid, complet, dar evitand pe cat posibil supraincarcarea. In general, elementele NiMH sunt mai sensibile la supraincarcare decat cele NiCd, asa incat utilizarea unui incarcator ieftin si mai vechi, poate produce pe termen lung, cheltuieli mai mari decat pretul unui incarcator 'inteligent'. Un incarcator pentru bateriile NiMH
ar trebui, in mod ideal sa indeplineasca urmatoarele conditii: Evenimente legate de incarcare Desi comportamentul la descarcare este similar cu elementele cu NiCd, celulele NiMH au un profil de incarcare foarte diferit, determinat de specificul electrochimic diferit al celor doua tipuri de baterii. Daca celulele NiCd se incarca endotermic, celulele NiMH degaja caldura la incarcare. Exista de asemenea, diferente legate de presiunea din celule ca si de curba tensiunii la borne. La atingerea capacitatii complete la incarcare (C = 100%), tensiunea la borne creste rapid si apoi scade lent, temperatura din element creste treptat iar presiunea creste rapid. La C>100% productia de hidrogen depaseste capacitatea de captare si inmagazinare a electrodului negativ; de asemenea, o mare parte din curentul care intra in celula este transformat in caldura. Continuarea incarcarii determina deschiderea ventilului de siguranta sau - daca acesta nu functioneaza- la distrugerea iremediabila a elementului. Pe de alta parte, capacitatea de incarcare se reduce semnificativ si proportional cu cresterea temperaturii din mediu, astfel incat incarcarea in conditii de temperatura ridicata reprezinta o problema.
Curentul de incarcare se evalueazaraportat la capacitatea bateriei si cel mai sigur este la < C/10, dar timpul necesar pentru incarcare devine intolerabil. Au fost proiectate incarcatoare rapide, care furnizeazacurent chiar la capacitate si care permit incarcarea intr-o ora! La incarcatoarele rapide insa, controlul supraincarcarii este extrem de important, avand in vedere cele expuse mai sus. Controlul supraincarcarii prin determinarea temperaturii pare a fi cea
mai buna metoda, in acest moment. Incarcatoarele moderne monitorizeazaatat
temperatura cat si tensiunea. La acestea, incarcarea se face in trei etape: Incarcatoarele mai ieftine incarca celulele in doua etape: Incarcatoarele in trei trepte sunt mai scumpe, deoarece includ sisteme
electronice mai complexe, dar protejeazacelulele la supraincarcare, astfel ca
pe termen lung, sunt mai economice.
Pastrarea bateriilor NiMH Toate celulele de acumulatori se autodescarca, datorita unor scurgeri parazite de curent in interior. Intrucat reactiile electrochimice sunt dependente de temperatura, modificari relativ mici ale temperaturii din mediu induce modificari importante in curba de descarcare. In general, o crestere cu 10 a temperaturii de mediu, dubleazarata autodescarcarii. La 60C bateria se autodescarca complet in 10 zile, in timp ce la 25C chiar si dupa 30 zile mai pastreaza peste 50% din capacitate. Recomandari de depozitare: - stocati bateriile
incarcate la cea mai redusa temperatura posibila (in frigider); Durata de viata In acest moment, celulele cu NiMH au o durata de viata (cicluri de incarcare-descarcare) similara cu cele cu NiCd, adica de 500 - 1000 cicluri, in conditiile unei intretineri corecte. Celulele de degradeazatreptat, prin oxidarea electrodului negativ - care induce o scadere a tensiunii la borne, si oxidarea electrodului pozitiv - care induce o reducere a capacitatii. Reducerea capacitatii impune reincarcarea precoce; reducerea tensiunii la borne insa poate impiedica functionarea consumatorului. Pentru a avea o durata maxima de viata, utilizatorul trebuie sa controleze incarcarea in ceea ce priveste: timpul si ritmul si sa evite supraincarcarea. Un mic grad de supraincarcare este util deoarece asigura incarcarea completa a bateriei dar mentinerea incarcarii la un curent mare pentru perioade lungi de timp reduc durata de exploatare a celulei. Intrucat temperatura ridicata accelereazatoate reactiile chimice, expunerea celulelor NiMH la temperaturi inalte accelereazasi procesul de imbatranire. Incarcarea in chargere de calitate modesta determina cresterea peste limitele acceptate ale temperaturii bateriilor si scurteazaciclul de viata. Supradescarcarea - imprejurare in care una dintre celulele bateriei isi inverseaza polaritatea - repetata de mai multe ori scurteaza in mod cert durata de viata. De asemenea, mentinerea in consumatori pe perioade lungi poate duce la supradescarcare si la scurgeri de electrolit. Masuri generale de protectie In general bateriile NiMH se
comporta foarte bine in exploatare, sunt rezistente la socuri de intensitate
mica, si au o durata lunga de viata. Totusi in timpul manipularii trebuie
respectate o serie de conditii: Elementele uzate, care se scot din
folosinta: |
Unitate scolara:Colegiul national "Bogdan Petriceicu Hasdeu"
Oras/Judet: Buzau/Buzau
Bibliografie: www.cadex.ro Cand a fost inventata bateria?
www.iem.pub.ro Energia fotovoltaica
www.gpbatteries.ro Acumulaturi li-ion
www.fotomagazin.ro Baterii NiMH
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 1825
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved