| CATEGORII DOCUMENTE |
| Alimentatie nutritie | Asistenta sociala | Cosmetica frumusete | Logopedie | Retete culinare | Sport |
TUMORILE VEZICALE
1.DEFINITIE
Tumorile vezicale sunt neoplazii care pot interesa fiecare structura a peretelui vezical, dar cel mai frecvent se descrie interesarea uroteliala ( circa 98 % ) .
2.CONCEPTII ACTUALE
Conceptiile actuale considera tumorile vezicii urinare drept o maladie foarte heterogena , cu potential biologic extrem de variabil de la o forma la alta si chiar pentru aceeasi tumora, imposibil de prevazut numai prin metode clinice, fara contributia histopatologului .
S-a remarcat faptul ca tumorile similare ca extensie clinica si diferentiere histologica se comporta foarte diferit de la un bolnav la altul , ceea ce aduce in discutie factorii de rezistenta la tumori, reactivitate imunologica etc. Astfel, o tumora papilara ramane singura manifestare la bolnavul respectiv pentru toata viata, in timp ce alta foarte asemanatoare macroscopic si microscopic, recidiveaza galopant si sfarseste rapid prin a deveni infiltranta .
In ultimii ani, ele tind la egalizarea repartitiei pe sexe si in acelasi timp interesand decadele mai mici de varsta, ceea ce constituie aspecte deosebite fata de cele cunoscute de generatia anterioara de urologi .
Aproape in totalitate tumorile vezicii urinare sunt de natura epiteliala maligna. Cele conjunctive de alta natura sau benigne sunt foarte rare, astfel ca vorbind despre tumorile vezicale, aproape de la sine inteles ne referim la cele uroteliale. De altfel, manifestarile lor clinice sunt aproape identice ceea ce simplifica diagnosticul de organ, dar impune diferentierea de structura .
S-a considerat mult timp ca tumora vezicala era consecinta grefarii pe mucoasa vezicala a celulelor neoplazice vehiculate de urina in sens descendent. Adica, tumora vezicala era fiica celei pieloureterale. S-a ajuns astfel la formularea teoriei multicentrice, care concepe aceste tumori ca o maladie a intregului uroteliu, aparand la intervale de timp diferite, datorita acelorasi impulsuri oncogenetice.[4].
3. INCIDENTA SI PREVALENTA
Vezica urinara este locul cel mai frecvent de dezvoltare al cancerului tractului urinar.
Incidenta in SUA, in anul 2000, a fost de 18 cazuri la 100.000 locuitori, raportul barbati/ femei fiind 3/1.[5]. Pentru barbati este al IV lea cancer ca frecventa in SUA (al V lea in Europa), reprezentand 5,5 % din totalul cancerelor.[5]. La femei ocupa locul al VII lea reprezentand 2,3 % din totalul cancerelor. In alte tari, incidenta cazurilor noi in anul 1996 a fost: 9.000 in Franta, 2.000 in Suedia, 8.000 in Spania si 1.120 in Belgia. [6,7,8,9]
Aproximativ 75-85% sunt limitate la mucoasa vezicala (Ta-Tis) sau submucoasa (stadiul T1). Restul de 15-25% au invadat muschiul vezicii urinare sau ganglionii limfatici (stadiul T2-4, N+) la prezentare. Incidenta cancerului a crescut cu varsta la ambele sexe, desi ne-am astepta la o crestere a incidentei mai mare la femei decat la barbati (speranta de viata la femei fiind mai mare cu 5 ani decat la barbati). [5,11,15]
Discrepanta intre incidenta cancerului la femei si la barbati este surprinzatoare, pentru ca
in ultimii 30 de ani femeile s-au alaturat babatilor in ceea ce priveste munca si obiceiurile, expunandu-se la numerosi carcinogeni industriali si ambientali (inclusiv fumatul), de care inainte erau ferite. Aceasta discrepanta poate fi explicata genetic, hormonal sau anatomic (retentia de urina la barbati datorata adenomului de prostata).[10,12].
Cancerul vezicii urinare este de circa doua ori mai frecvent la caucazieni fata de negri pentru sexul masculin si de 1,5 ori pentru sexul feminin.[13,14].
Este un lucru deja demonstrat faptul ca riscul crescut de cancer la albi este limitat la tumori non-invazive, pe cand la populatia de culoare, riscul este determinat de un diagnostic tardiv si de forme mai agresive de cancer.
In ceea ce priveste prevalenta, cancerul vezicii urinare este pe locul al IV lea pentru toate
decadele de varsta la barbati si pe locul al II lea pentru adultul de varsta mijlocie si varsta
a III a.[14].
4. ETIOPATOGENIA TUMORILOR VEZICALE
Spre deosebire de majoritatea neoplasmelor umane, al caror mecanism de aparitie este inca incert, unele neoplasme vezicale recunosc cauze bine determinate de aparitie. Inca din 1894 Rehn a descris actiunea cancerigena a anilinei, paratoluidinei si metatoluidinei asupra uroteliului prin derivatul N-aminodifenil.
Observatiile lui au fost ulterior pe deplin confirmate la muncitorii din fabricile de coloranti, in industria chimica, a cablurilor electrice, in industria cauciucului, la curatatorii de canale, la muncitorii care lucreaza cu smoala fierbinte sau manevreaza otrava de soareci si chiar la lucratorii in piele, frizeri sau surori medicale.
In procesul de productie sunt expusi la contactul prelungit cu substante cancerigene, dintre care 4 sunt bine cunoscute ( 4-aminodifenil, β-naftolamina, benzidina, auramina), iar alte 5 sunt suspectate ( n-nitrodifenil, magenta, dianisidina, 3.3-diclorbenzen si 0-toheidina ).
Actiune cancerigena uroteliala mai au si triptofanul, ortoaminotoluenul si 2-acetilaminofloruenul.
Aminele cancerigene, dintre care cea mai puternica este β-naftolamina, patrund in organism pe cale digestiva sau respiratorie, sunt degradate in ficat prin glicurono-conjugare in ortoaminofenil care se elimina prin rinichi, unde sub influenta β-glicuronidazei se transforma in ortofenol cancerigen.
Tumorile uroteliale apar de obicei dupa expuneri de aproximativ 7-10 ani la actiunea substantelor amintite. Pentru carcinogeneza este necesar contactul prelungit al acestora cu mucoasa vezicala (de unde se poate deduce rolul favorizant al obstacolelor cervicouretrale in geneza tumorilor vezicale si frecventa lor in asociere cu adenomul de prostata ).
Sunt cunoscute si alte conditii care cresc activitatea β-glicuronidazei, cu stimularea carcinogenetica consecutiva si anume :
intensificarea cu bilharizia, care pe langa actiunea metabolitilor cancerigeni, asociaza actiunea iritanta a oualor parazitului, actiune iritativa a infectiei urinare si cea toxica;
infectiile vezicale cu pH alcalin;
fumatul excesiv, care determina cresterea concentratiei urinare a metabolitilor cancerigeni ai triptofanului, dar si aparitia altor cancerigeni vezicali cum sunt benzopirenul si N-nitrosonornictonina;
activitatea β-glicuronidazica a urinei mai poate fi crescuta in litiaza urinara, adenomul de prostata, chistul renal, alte cancere si chiar in cursul curei de diureza, ceea ce poate explica unele coexistente intre tumorile vezicale si alte afectiuni ale aparatului urinar;
intre medicamentele care ar favoriza carcinogeneza vezicala, se citeaza opiul, substantele anticancerigene alchilante si fenacetina. Relativ la ultima mentionam ca metabolitii acesteia sunt asemanatori cu cei de naftilamine.
In carcinogeneza vezicala au mai fost incriminati unii factori alimentari (hipelcolesterolemie, regimul excesiv de grasimi), unele saruri de metale grele, apa potabila care contine triolmetal, cafeaua decafeinata cu tricloretiliu, nitrosaminele provenite din degradarea nitritilor utilizati in conserve, ca si aditivi alimentari cum sunt zaharina, ciclamatii si substantele edulcorante de tipul xilitolului.
Infectiile vezicale cronice care se insotesc de crestere nitrozaminelor endovezicale, litiaza vezicala si in general toate iritatiile vezicale cronice, la care se adauga staza urinara si infectia, cum sunt cistitele cronice, diverticoli vezicali, mucoasa vezicala expusa diverselor agresiuni, ca in extrofia vezicala, sunt considerati drept factori predispozanti pentru carcinogeneza vezicala.
Se mai adauga metaplaziile malpighiene, cunoscute sub numele de plagi leucoplazice, cistita chistica sau degenerescenta chistica a mucoasei, cistita glandulara, leziunile preneoplazice ale mucoasei vezicale care trebuie supravegheate cu atentie.
Recent a fost propusa o teorie a invaziei neoplazice uroteliale in 3 pasi:
Initial, celulele tumorale sunt legate de membrana bazala. Se descriu astfel receptorii pentru laminina. Numarul receptorilor este mai crescut in cazul tumorilor invazive.
Dupa aderarea la membrana bazala incepe degradarea acesteia prin secretia de proteaze.
Progresia tumorii este completata prin secretia de citokine care contribuie la mobilitatea celulara si eventual la metastazare. Concentratia factorilor mobilitatii autocrine din urina este crescuta la pacientii cu tumori invazive.[4].
4.1 FACTORII DE RISC
In categoria factorilor de risc ai cancerului vezicii urinare intra expunerea ocupationala la diverse substante chimice, fumatul,[16,17,18,19], alcoolul,[20,21,22,23], excesul de cafea,[24,25], dieta,[26,27], ingestia de analgezice sau indulcitori artificiali,[28], diverse infectii virale, bacteriene si parazitare,[29], cistite recurente,[30,31], litiaza vezicala, HPV [32] si tratamentul citotoxic. Carcinogenii produc alterari la nivelul ADN-ului celulei tinta (in acest caz celulele epiteliale tranzitionale) initiind si propaganda procesul tumoral.
4.2 ASPECTE GENERALE MOLECULARE SI GENETICE IN CARCINOGENEZA TUMORILOR VEZICALE
La aparitia cancerului vezical contribuie diferiti factori carcinogeni si de risc. De exemplu, beta-naftilamina, un component din fumul de tigara este un important factor carcinogen, iar fumatorii au un risc de 4 ori mai mare sa dezvolte un cancer urotelial decat nefumatorii.O incidenta mare a carcinoamelor uroteliale s-a gasit si la muncitorii din industria cauciucului care sunt foarte expusi la beta-naftilamina, benzidina, fenacetina si ciclofosfamida.
In cele mai multe tipuri de cancer, inclusiv in cancerul vezical, transformarea dintr-o celula normala intr-una maligna se face printr-un mecanism pas-cu-pas.
Secvential, expresia diferitelor clase de gene (oncogene, gene tumorale, gene ale ciclului celular si gene de reparare a AND-ului) sunt alterate. Aceste alterari implica mutatii sau aberatii cromozomiale (translocatii, insertii, amplificare, deletie). Deletiile anumitor regiuni cromozomiale joaca un rol cheie in patologia moleculara a cancerului vezical, prin modificarile pe care le determina in genomul celulei normale. [33,34].
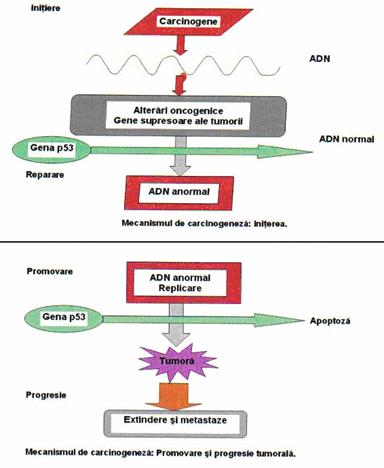
Fig.2 Mecanismul carcinogenezei. [33]
Agentii carcinogeni sunt impartiti in 3 categorii:
1.initiatori - doar initiaza transformarea tumorala, suficienta insa pentru expresia in
continuare a fenotipului malign.
2. promotori - induc direct si indirect alte transformari genetice aditionale cu efect de
extindere a fenotipului malign.
3. de progresie - ajuta la dobandirea de noi proprietati ale celulelor canceroase
necesare in cresterea tumorala (mitogeneza), sustinerea unui flux sanguin tumoral adecvat invaziei tesuturilor vecine.[33].
4.3 FACTORII DE CARCINOGENEZA IN TUMORILE VEZICALE
tutunul
beta-napftylaminele
4-aminodiphenil chloronaphazine
schistosomiaza
ciclofosfamida
fenacetina
litiaza
urina
iritatiile cronice
obstructiile subvezicale
benzidine
auramine
zaharina (ciclamatii)
cafeaua
radiatiile
grasimile si uleiurile dietetice
deficitul de vitamina A
nitrati, nitriti, nitrosamine
infectiile tractului urinar
triptofanul
azatioprina
opiul
virusuri
hormoni
gazele de esapament [35].
4.4 ONCOGENELE IN TUMORILE VEZICALE
Cele mai importante oncogene implicate in cancerul vezicii urinare sunt:
a). ras
b). receptorul factorului de crestere epidermal (EGFR)
c). erb-B-2
Potentialul de transformare a oncogenelor ras se datoreaza unei mutatii, in timp ce, celelalte doua sunt exprimate in exces in celulele transformate.
a) Familia de gene ras este formata din:
Ha-ras
K-ras
N-ras
Toate aceste proteine sunt similare din punct de vedere biochimic si au potential oncogenic. Dintre toate, doar mutatiile genei Ha-ras sunt importante in carcinogeneza din cancerul vezical.[34,36].
b) Proto-oncogenele erb-B-2 si EGFR (receptorul pentru factorul de crestere) apartin "superfamiliei" de receptori de tirozin-kinaze.[36]. EGFR este activat de EGF si intervine in transformarea factorului de crestere alfa (TGF-alfa). Acest lucru duce la dimerizare, schimbarea conformatiei si autofosforilare a receptorului. In uroteliul normal celulele EGFR pozitive sunt concentrate spre membrana bazala iar in uroteliul malign EGFR este exprimat in toata grosimea uroteliului, de la membrana bazala spre suprafata, interesand toate tipurile de celule epiteliale.[34].
c) Erb-B-2 este o oncogena care codifica pentru receptorul unui factor de crestere, ca si EGFR. Amplificarea si expresia in exces a erb-B-2 are un rol mai mic in cancerul vezical.[34].
4.5 GENELE SUPRESOARE TUMORALE
Cancerul este definit ca o boala in care celulele normale se modifica, se divid necontrolat, cresc foarte repede dand nastere unei mase tumorale.[37].
Primul set de gene este cunoscut ca proto-oncogene, iar al doilea, cunoscut ca gene supresoare tumorale, este incriminat in inhibarea cresterii celulare si pare ca are consecinte in protectia impotriva aparitiei cancerului.[38].
Gena retinoblastomului (Rb) si proteina p53 sunt, probabil, cele mai importante gene din grupul genelor supresoare tumorale.[39]. Ambele gene sunt implicate in controlul ciclului celular si joaca un rol cheie in carcinogeneza cancerului de vezica .[39,40].
Sunt reprezentate de:
- gena retinoblastomului
- proteina p53
- gena CDKN2
-alte aberatii genetice.
a). Gena retinoblastomului (Rb) a fost prima gena supresoare tumorala descoperita, al carei produs este o fosfoproteina nucleara. Ea se localizeaza in banda q14, pe cromozomul 13 (13ql4) si fosforilarea ei joaca un rol important in reglarea ciclului celular.[34,40,41].
Exista o corelatie puternica intre inactivarea genei Rb si stadiul tumorii, astfel tumorile Rb-negative invadeaza musculara pe cand cele Rb-pozitive raman superficiale.
Inactivarea genei Rb este o deletie a cromozomului 13q.
Fosforilarea este o modificare covalenta reversibila, catalizata de protein-kinaze. Nu numai in cazul genei Rb ci si intr-o larga varietate de alte proteine, fosforilarea este o modalitate generala de reglare a activitatii proteice.[34,40].
b). Proteina p53 este tot o fosfoproteina nucleara care a fost descoperita pentru prima data in celulele rozatoarelor, transformate de virusul simian SV40. Aceasta transformare a dat nastere complexului intre antigenul T-viral si proteina p53, ducand la o scadere a ratei de degradare in ferarea celulara. [34,42,43,44,45,].
In mod normal, cantitatea de proteina p53 in celule este foarte mica. Proteina nu este initiata in asigurarea functiilor normale ale celulelor, dar isi gaseste importanta in anumite instante.
Gena p53 blocheaza ciclul celular in faza G1 si permite separarea AND-ului alterat, fiind un pas initial in replicarea AND-ului.[34,44,45].
c) Gena CDKN - deletii ale cromozomului 9p si genele ciclului celular p15 si p16.
CDKN 2 a fost identificata ca o gena localizata in regiunea 9p21 si este modificata in majoritatea tumorilor vezicale. Ea pare sa fie responsabila pentru cele mai multe din efectele induse prin deletia 9p21. De asemenea, codifica o proteina de 16 KD (proteina p16). [34,46].
Aceasta proteina este un inhibitor al kinazei 4, dependenta de ciclina si regleaza fosforilarea genei Rb. Pierderea proteinei p16 duce la fosforilarea necontrolata a genei Rb prin complexe ale ciclinei si kinaza dependenta de ciclina. Gena CDKN este un pas important in dezvoltarea unei tumori vezicale reprezentand singura alterare genetica in multe tumori superficiale cu grad mic de displazie.
d) Alte aberatii genetice. S-au mai observat, in toate tumorile vezicale cu grad mare de displazie, deletii in cromozomul 1Ip. De asemenea, deletia bratului scurt al cromozomului 8 a aratat o asociere puternica cu un grad mare de displazie si stadiu avansat al tumorilor vezicale, in proportie de 23% din toate tumorile si in proportie de 53% din tumorile cu invazie musculara.[34].
5.FACTORII DE PROGNOSTIC IN CARCINOAMELE UROTELIALE
6. CLASIFICAREA TUMORILOR VEZICALE
A. TUMORI EPITELIALE (UROTELIALE) BENIGNE
a) Papilom tipic
b) Papilom inversat
c) Papilom scuamos
d) Condilom acuminat
e) Adenom vilos
f) Chistadenom mucinos [49]
B. TUMORI EPITELIALE (UROTELIALE) MALIGNE
a) Carcinom in situ urotelial
b) Carcinom scuamos
c) Adenocarcinom
d) Carcinoame nediferentiate [49].
CIS urotelial se exprima prin anomalii citoarhitecturale ale uroteliului, interesand intreaga grosime.
Evolutia CIS urotelial izolat este mai putin agresiva decat daca ar fi asociat cu o tumora papilara.
Leziunile uroteliale pot fi plane sau papilare. De mai bine de 50 de ani tumorile uroteliale
ale vezicii urinare sunt impartite in "tumori superficiale" si "tumori invazive".
Astfel se disting tumorile limitate la mucoasa, care pot fi tratate endoscopic, de cele care
invadeaza musculara proprie.[50].
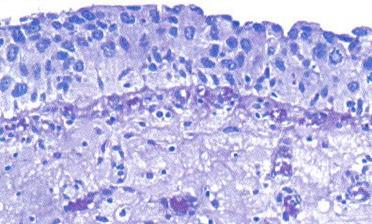
Fig.3 Carcinom in situ (HEx10) [51].
C. TUMORI MEZENCHIMALE
a) Tumori mezenchimale benigne: leiomioame, hemangioame, limfangioame,
neurofibroame, schwannoame, histiocitoame fibroase benigne si lipoame.
b) Tumori mezenchimale maligne: leiomiosarcom, rabdomiosarcom, fibrosarcom.[49].
D. TUMORI MIXTE
a) Tumori mixte benigne: adenofibroame
b) Tumori cu grad scazut de malignitate: adenosarcom
c) Tumori mixte maligne: carcinosarcoamele.[49,50].
E. ALTE TUMORI PRIMITIVE VEZICALE
a) Paragangliomul
b) Melanomul malign primitiv
c) Chist dermoid
d) Choriocarcinom
e) Tumora vitelina [49].
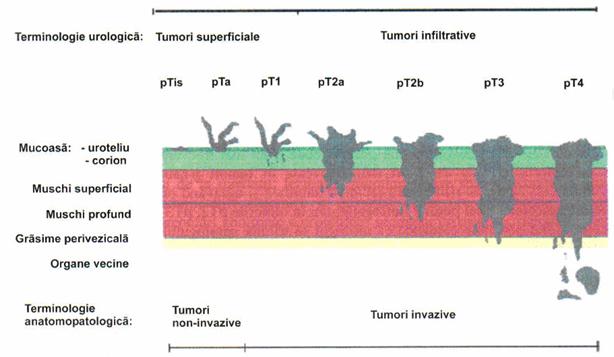
Fig.4. Stadierea patologica (p) a tumorilor maligne vezicale
Macroscopic, tumorile vezicale se clasifica in 3 grupe mari: pediculate, sesile si infiltrante .
Tumorile pediculate se prezinta ca excrescente ale mucoasei vezicale de culoare rosietica, unice sau multiple, cu franjuri fine, scurte sau lungi, flotand in mediul vezical implantate parietal printr-un pedicul subtire si inconjurate de o mucoasa vezicala cu aspect normal. Cand sunt foarte multe, pot ocupa aproape toata endovezica, realizand forma clinica de maladie viloasa vezicala. [51].
2. Tumorile sesile se prezinta fie cu caracterele de mai sus, insa cu baza larga de implantare, fie sub o forma care le apropie mai curand de tumorile solide, mai inchise la culoare, cu franjuri scurte, mai putin mobile sau chiar " inghetate ", uneori ulcerate. Mucoasa peritumorala apare adesea cu modificari congestive, edematoase, sugerand agitatie microscopica.[51].
3. Tumorile infiltrative sunt tumori vegetante sau infiltrant-ulcerate, cu baza larga de implantare in peretele vezical cu suprafata mamelonata, neregulata, murdara ulcerata, cu zone de hemoragie si necroza. Mucoasa din jur este aglutinata spre baza tumorii, edematoasa, cu picheteu hemoragic. Uneori se pot observa excrescente si modificari parietale la distanta de tumora sugerand extensia tentaculara submucoasa.[51].
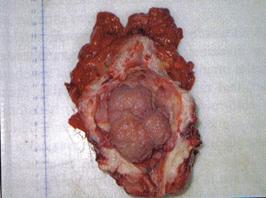 a
a 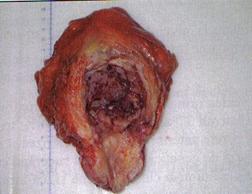
Fig.5 Piese de cistectomie: a)tumora solida, b) tumora vegetanta sesila; [51].
 b
b 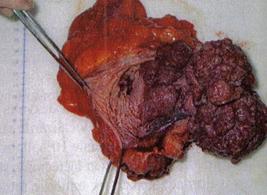
Din punct de vedere microscopic, tumorile vezicale uroteliale au fost impartite ( Galiau si Morice ) in carcinoame si tumori paramalpighiene.Carcinoamele sunt subdivizate in:
- epitelioame epidermoide,
- adenocarcinoame ,
- epitelioame nediferentiate,
- epiteliomul in situ.
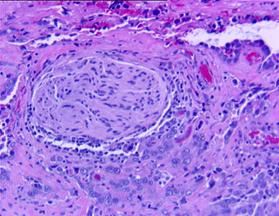
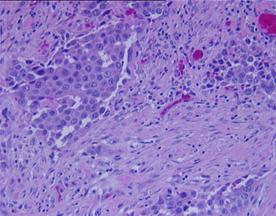
a) b)
Fig.6 Aspecte microscopice. a) Carcinom urotelial cu grad inalt de malignitate (Hex10) b) Invazie tumorala in intesitiile muscularei propii. (Hex5). [51].
Clasificarea Mastofi:
A. Papiloame cu celule tranzitionale (paramalpighiene): tumori benigne compuse din 6-7 straturi de celule uroteliale normale. Singurul element tumoral este pluristatificatia.
B. Papiloame cu celule tranzitionale de tip invers, dezvoltate cu probabilitate din cuiburile celulare von Brn, care de obicei sunt cantonate pe marginea posterioara a colului vezical si in uretra prostatica.
C. Papiloame epidermoide, asemanatoare condiloamelor acuminate .
D. Carcinoame tranzitionale, care sunt tumori cu potential invaziv, prezentand in grade variabile celule nediferentiate, de unde a rezultat impartirea lor in carcinoame tranzitionale de gradul 1(G1) care sunt neinvazive, de gradul 2(G2) tot neinvazive si de gradul 3 (G3) care au o subvarianta invaziva .
E. Variante de carcinoame tranzitionale, subdivizate in carcinoame cu metaplazie epidermoida, cu metaplazie glandulara si mixte (epidermoide +glandulare).
F. Carcinoamele epidermoide pure, sunt tumori ulcero-infiltrante cu populatie celulara omogena (celule keratinizate des asociate cu iritatii vezicale cronice si parazitoze de tip Bilharzia).
G. Adenocarcinoamele mucosecretante sunt relativ rare (2% din toate tumorile uroteliale ) si se dezvolta fie primitiv in vezica, din plaje de cistita glandulara sau la pacientii cu extrofie vezicala, fie secundar, la nivelul calotei din epiteliul uracai.
H. Carcinoamele nediferentiate sunt tumori maligne cu grad mare de anaplazie.[51].
7. STADIALIZAREA TUMORILOR VEZICALE
CLASIFICAREA TNM IN CANCERUL VEZICAL
Tumora primara (T)
Specimenul TUR-V trebuie sa contina musculara.
Tx Tumora primara nu poate fi evaluata
T0 Nu exista evidente asupra tumorii primare
Tis Carcinom in situ
Ta Carcinom papilar neinvaziv
T1 Tumora invadeaza tesutul conjunctiv subepitelial
T2 Tumora invadeaza musculara
T2a Tumora invadeaza musculara superficiala (jumatatea interna )
T2b Tumora invadeaza musculara profunda (jumatatea externa)
T3 Tumora invadeaza tesutul perivezical
T3a Microscopic
T3b Macroscopic (masa extravezicala)
T4 Tumora invadeaza oricare dintre urmatoarele:prostata, uter, vagin, perete abdominal
T4a Tumora invadeaza prostata, uterul sau peretele vaginal
T4b Tumora invadeaza peretele pelvin sau abdominal
-"m"- arata leziuni multiple oricarei categorii T
-"is"- arata carcinomul in situ asociat oricarei categorii T.
Ganglionii limfatici regionali (N)
(Ganglionii limfatici pelvini sub bifurcatia arterei iliace comune)
Nx Ganglionii limfatici regionali nu pot fi evaluati
N0 Nu exista metastaze in ganglionii limfatici regionali
N1 Metastaza intr-un singur ganglion limfatic cu cea mai mare dimensiune de 2 cm
N2 Metastaza intr-un singur ganglion limfatic cu cea mai mare dimensiune > 2 cm si
<5 cm, sau ganglioni limfatici multipli, nici unul mai mare de 5 cm
N3 Metastaza intr-un ganglion limfatic cu cea mai mare dimensiune >5 cm.
Metastaze la distanta (M)
Mx Prezenta metastazelor la distanta nu poate fi evaluata
M1 Fara metastaze la distanta
M2 Metastaze la distanta.
Cerinte pentru clasificarea pTNM
pT Examinarea histologica a piesei de cistectomie partiala sau totala
pN0 Examinarea histologica a peste 8 ganglioni limfatici regionali
pN1 Confirmarea microscopica a uneia sau mai multor metastaze in ganglionii limfatici
<2 cm
pN2 Idem, dar >2 cm, sau metastaze microscopice in 2 sau mai multi ganglioni limfatici
pN3 Metastaze in 2 sau mai multi ganglioni limfatici regionali, idem dar >5 cm
pM1 Dovada histologica sau citologica de metastaza la distanta.[4].
Stadializarea TNM
|
Stadiul 0 |
0a |
Ta |
No |
Mo |
|
0is |
Tis |
No |
Mo |
|
|
Stadiul 1 |
T1 |
No |
Mo |
|
|
Stadiul 2 |
T2 |
No |
Mo |
|
|
Stadiul 3 |
T3a |
No |
Mo |
|
|
T3b |
No |
Mo |
||
|
Stadiul 4 |
T4 |
No |
Mo |
|
|
orice |
T |
N1 |
Mo |
|
|
orice |
T |
No |
Mo |
|
|
orice |
T |
N2 |
Mo |
|
|
orice |
T |
orice N |
M1 |
Tabel nr. 7 - stadializarea TNM.[52].
8. DIAGNOSTICUL TUMORILOR VEZICALE
8.1 SEMNE SI SIMPTOME
Hematuria este cel mai frecvent simptom, este nedureroasa si prezenta la aproximativ
85% dintre pacienti. Hematuria este frecvent intermitenta.
Piuria se intalneste rar, dar prezenta ei tradeaza tumori infiltrative, ulcerate, sfacelate, necrozate, cu supuratie asociata.
Polachiuria este inconstanta, apare in formele infiltrative, in general este semn de etapa tardiva in evolutia tumorilor vezicale.
Disuria se poate constata drept consecinta a infiltrarii colului vezical si se poate manifesta
izolat sau asociat cu simptomele descrise mai sus.
Durerea pelvina este semnul sugestiv de infiltratie tumorala pelvina sau metastaze in
oasele bazinului.
Cistita tumorala este sindromul cvasicaracteristic al tumorilor vezicale avansate, cu
aparitie tardiva, rezultat din invazia detrusorului, supuratia tumorii si infiltratiile
neoplazice parietale.[53].
8.2 EXAMENUL LOCAL
Consta in inspectia si palparea abdomenului, dar mai ales din examinarea vezicii urinare
prin palparea hipogastrului combinata cu tactul rectal sau vaginal. Bolnavul va fi examinat in pozitie ginecologica, cu vezica goala. Cele mai complete date le obtinem daca bolnavul este anesteziat si miorelaxat.
Tumorile papilare mici nu pot fi palpate. Cele mari se prezinta ca o masa imprecise delimitata in interiorul vezicii, mobila, de regula nedureroasa.
Infiltratia incipienta schimba consistenta peretelui vezical, pe care il face ferm, elastic, in timp ce induratia profunda se prezinta ca un nodul sau o zona dura, neregulata, cu margini imprecise.[53].
8.3 INVESTIGATII DE LABORATOR
a) uzuale - hematologice, hepatice, metabolice
b) specifice - citologia urinara exfoliativa, testul de inhibitie a aderentei limfocitare
si markeri de diagnostic. [51].
8.4 INVESTIGATII IMAGISTICE
a) Radiografie renovezicala simpla (RRVS) si urografie intravenoasa (UIV)
b) Ecografie vezicala
c) Tomografie computerizata
d) Imagistica prin rezonanta magnetica nucleara (IRM)
e) Radiografie osoasa si toracopulmonara, scintigrafie ososasa (pentru metastaze)
f) Cistoscopia ascendenta sau retrograda
g) Arteriografia vezicala
h) Flebografia pelviana
i) Detectarea tumorilor vezicale prin fluorescenta
j) Biopsia vezicala: examenul histopatologic pune diagnosticul de certitudine. [36,54,55,56].
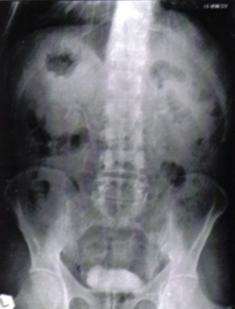
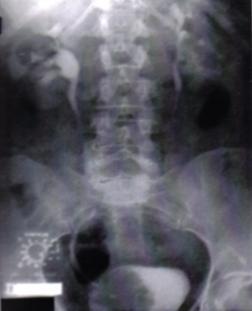
Fig.8 Imagini lacunare in aria vezicii urinare sugerand tumori vezicale superficiale [51].
9. DIAGNOSTICUL DIFERENTIAL
Pentru etapa pre-endoscopica de investigatie si diagnostic amintim: tuberculoza urinara
proliferativa, cistitele hipertrofice, cheaguri endovezicale.
Diagnosticul diferential imagistic si endoscopic se face cu: litiaza vezicala radiotransparenta, ureterocel bilateral, tuberculoza urogenitala, corpii straini intravezicali
calcificati, tumori vezicale benigne.[57,56].
10. TRATAMENTUL TUMORILOR VEZICALE
PROTOCOLUL ASOCIATIEI ROMANE DE UROLOGIE
a. Rezectia transuretrala cu biopsii de pat si de margini tumorale
b. Tratament institutional cu BCG sau citostatice
c. Electrorezectia transvezicala
d. Laser-vaporizarea
e. Alte operatii: chirurgie deschisa.[58].
Parametrii cu valoare prognostica pentru recidiva, in ordine descrescatoare sunt:
Numarul tumorilor prezente in momentul diagnosticului .
Rata recidivelor; o recidiva la 3 luni.
Dimensiunile tumorii: o tumora voluminoasa are sanse de recidiva mai mare.
Gradul de anaplazie.[59].
10.1 TRATAMENTUL ENDOSCOPIC
A) REZECTIA TRANSURETRALA SAU/SI FULGURATIA
Metoda de electie in tratamentul tumorilor vezicale este rezectia endoscopica transuretrala (TUR-V). Se recomanda biopsii randomizate mai ales in caz de tumori multiple si mai mari de 3 cm.[36].
A. Tehnica rezectiei standard
Distingem 3 modalitati de efectuare:
Rezectia orizontala sau paralela- este practicata in cazul tumorilor de marime mijlocie, solitare, situate la distanta de orificiile ureterale. Indepartarea tesutului tumoral se face in straturi succesive, suprapuse, paralele cu baza tumorii. Se ajunge, treptat la baza tumorii ce se va putea rezeca corect, cu hemostaza adecvata.
Rezectia verticala- consta in indepartarea tumorii de sus in jos, pe un ax perpendicular pe baza tumorii. Frecvent aceste doua metode se folosesc asociat.
Rezectia primara a pediculului- utilizata in cazul tumorilor mici, papilare, pediculate, atunci cand abordarea pediculului se poate face din lateral.[60].
B.Rezectia transureterala de tip diferential (TURV-D)- Biopsia Bressel
Permite reconstructia fidela a tumorii vezicale si poate depista daca tumora a fost indepartata in totalitate sau daca persista tesut tumoral in una din cele 6 fragmente rezecate.
Tehnic, se efectueaza in felul urmator:
se rezeca partea exofitica a tumorii (esantionul 1);
se rezeca din marginile patului tumoral, orele 12,3,6,9 (esantioanele 2,3,4,5) pentru a evidentia tesutul tumoral restant;
se efectueaza o biopsie din centrul patului tumoral (esantionul 6).
Cele 6 esantioane se examineaza de catre anatomo-patolog. Daca unul dintre esantioane este pozitiv se repeta rezectia, in acelasi maniera, din zona respectiva.
Limitele rezectiei endoscopice transureterale sunt date de:
imposibilitatea pasajului prin uretra (stricture, cai false, tumori prostatice voluminoase)
localizarea tumorii intr-o zona greu accesibila (perete vezical anterior in imediata vecinatate a colului vezical)
tumora situata in diverticul vezical (risc mare de perforatie vezicala)
asocierea tumorii cu alte leziuni (litiaza vezicala multipla sau voluminoasa)
purtatorii de stimulator cardiac (risc de dereglare a acestuia).[60].
Complicatiile rezectiei endoscopice transureterale pot fi:
sindromul post-TURV - se datoreaza resorbtiei unei cantitati mari de lichid de spalare in circulatie sanguina, conducand la cresterea valorilor tensiunii arteriale, tahicardie, dispenee si falsa anemie (prin dilutie mare).
infectie urinara - apare ca urmare a nerespectarii regulilor de asepsie si antisepsie in timpul operatiei.
hemoragie masiva - este controlabila endoscopic, prin electrocoagulare locala.
perforatie vezicala - poate fi subperitoneala sau intraperitoneala. Daca perforatia este mare rezolvarea trebuie facuta imediat prin chirurgie deschisa.
rezectie incompleta a tumorii - este cea mai grava complicatie a rezectiei endoscopice.[60].
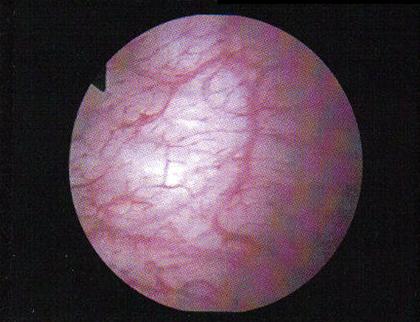
Fig. nr.9 Aspect endoscopic normal al mucoasei vezicii urinare [61].
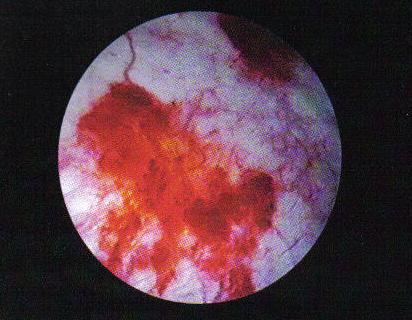
Fig. nr. 10 Ulceratia mucoasei vezicii urinare. Aspect endoscopic [61].
Avantajele acestei metode (TURV-D) constau in posibilitatea efectuarii sub analog-sedare in doze mici, utilizarea unui instrumentar mai fin ce traumatizeaza mai putin mucoasele si efectuarea hemostazei concomitant cu vaporizarea tumorii, ceea ce ar conduce la minimalizarea posibilitatii de diseminare a celulelor tumorale pe cale hematogena. Cel mai folosit LASER este Neodymium-YAG. Dezavantajul major al acestei metode este dat de imposibilitatea recoltarii de specimen tumoral pentru examenul histopatologic.[51,61].
B) CISTECTOMIA
Cistectomia totala este rar necesara la pacientii cu tumori superficiale; exceptie fac doar tumorile papilare nerezecabile sau/si carcinoamele in situ care nu raspund la terapia intravezicala.[62].
Indicatiile cistectomiei la pacientii cu tumori vezicale Ta, T1, Tis sunt: pacient de varsta tanara, cu tumora multifocala, grading 3, Tis concomitent, pozitionata intr-o zona greu de rezecat (perete anterior, posterior) cu T1 cel putin la re-TURV, recurenta sub BCG.[63,64,65].
La pacientii cu tumori de grad mare, tumori superficiale cu recurenta crescuta sau Tis, la momentul cand se ia in calcul cistectomia, aproximativ 1/3 aveau evidente microscopice de stadiu mai avansat si aproximativ 1/2 din pacientii cu stadiu crescut aveau deja extensie exravezicala sau metastaze.[63,64].
In concluzie, cu cat cistectomia (la pacientii cu grad crescut) se efectueaza mai repede, cu atat posibilitatea de vindecare este mai mare.[66,67,68].
10.2 TRATAMENUL ADJUVANT INSTITUTIONAL
Diferitele forme de complementaritate terapeutica urmaresc:
prevenirea aparitiei recidivelor sau
prelungirea intervalului de timp in aparitia recidivelor si,
eventual, scaderea grading-ului;
prevenirea sau intarzierea progresiei.[36,69].
Posibilitati in tratamentul adjuvant:
terapia institutionala
imunoterapie institutionala
chimio-imunoterapie intravezicala. [69].
Indicatiile terapiei intravezicale includ urmatoarele:
1. Tumori primare multiple
2. Recidive tumorale multiple
3. Grading tumoral mare- G3
4. Tumori in stadiul T1
5. Citologie urinara pozitiva post-TUR-V
6. Displazie sau Cis in biopsiile randomizate.[69].
10.3 IMUNOTERAPIA INTRAVEZICALA CU BCG
Bacilul Calmette-Guerin sau BCG, preparat din Mycobacterium bovis, este in mod curent cel mai activ imunoterapeutic pentru uz intravezical si este considerat ca tratament de prima linie la pacientii cu tumori vezicale superficiale agresive T1G3 si CIS.[70,71,72,36].
Exista doua premize de certitudine:
este necesar contactul direct intre BCG si celulele tumorale si
este necesara prezenta limfocitelor T (CD4 helper si CD8 citolitice) pentru activitatea antitumorala mediata de BCG.[70].
Contactul direct intre BCG si celulele tumorale este necesar pentru a permite atasarea bacteriei la celulele tumorale si la mucoasa vezicala, prin intermediul fibronectinei. Bacilii sunt inclusi prin fagocitoza activa, atat in uroteliul normal cat si in celulele tumorale. Celulele prezinta antigenul de suprafata al limfocitelor T care initiaza o cascada de evenimente imunologice locale si sistemice:[73,74].
specifice- implicand anticorpi si componente imune celulare;
nespecifice- citokine asociate cu reactia de hipersensibilitate de tip intarziat, celule natural killer,celule killer activate de limfokine.
10.4 TRATAMENTUL RECIDIVELOR
Se incepe cu schema initiala. In cazurile cu recidive multiple sau de risc mare se trece pe BCG. Chimioterapia institutionala intravezicala se face cu Mitomycin C, Epirubicin sau Adriamicin.[38].
PARTEA SPECIALA
INTRODUCERE
Lucrarea de fata isi propune sa demonstreze ca utilizarea vaccinului BCG in instilatii endovezicale in tratamentul tumorilor vezicale superficiale permite scaderea ratei recidivelor tumorale, consolidarea terapiei chirurgicale si chiar vindecarea pacientului; deci cu alte cuvinte sa demonstreze eficienta tratamentului instilational in tumorile vezicale superficiale.
Abordarea teoretica a acestei teme si studiul practic pe caziustica oferita de Clinica de Urologie a Spitalului Clinic Judetean de Urgente Sibiu, este justificata de incidenta crescuta a tumorilor vezicale, indeosebi superficiale si de faptul ca pacientii pot urma tratamentul instilational cu rezultate maximale.
STUDIU CLINIC
TRATAMENTUL BCG
Cu toate ca din punctul de vedere al tolerantei, efectele secundare ale chimioterapiei intravezicale sunt mult mai blande si mai rare, imunoterapia intravezicala a dovedit rezultate net superioare in tratamentul tumorilor vezicale superficiale, indiferent de stadiu.
Bacilul Calmette-Guerin sau BCG, preparat din Mycobacterium bovis, este in mod curent cel mai activ agent imunoterapeutic pentru uz intravezical si este considerat ca tratament de prima linie la pacientii cu tumori vezicale superficiale agresive T1G3 si Cis.[70,73,74].
De la introducerea BCG in practica urologica, impactul acestei terapii asupra managementului tumorilor vezicale superficiale a fost atat de puternic incat si acum, poate fi considerat cea mai de succes terapie din toate imunoterapiile aplicate si de asemenea, ca una din cele mai importante etape in controlul acestor neoplasme.
Dar in ciuda raspandirii largi a acestiu tratament, modul prin care BCG isi exercita activitatea antitumorala nu este inca bine inteles si inca nu se cunoaste cine sau ce omoara celulele neoplazice.
Dupa instilatii, se pot produce ulceratii ale mucoasei sau granuloame, in care s-au identificat limfocite CD4. De asemenea, in urina se identifica interleukina 2 (IL2). Vaccinul BCG are atat efect terapeutic cat si profilactic.[38,70].
Analize sistematice ale raspunsului imun local in vezica urinara au fost facute in mai multe studii. Tehnicile folosite au inclus analize imunochimice ale subpopulatiilor celulare, infiltrate de citokine detectabile local si analize ale urinii pacientului pentru a determina secretia de citokine. Aceste studii au caracterizat raspunsul imun local imediat si pe termen lung, la pacintii cu imunoterapie intravezicala cu BCG. [74].
Raspuns complet la BCG apare la aproximativ 40-80% din pacientii cu tumori vezicale superficiale reziduale.
Dintre efectele adverse se pot nota:
hematurie
disurie
polakiurie
cistita hemoragica.
Daca simptomele sistemice sunt severe, instilatiile trebuie oprite.
La pacientii cu febra prelungita, prostatite granulomatoase sau infectie sistemica se administreaza Izoniazida (600 mg/zi) si Rimfapicina (600 mg/zi). Pacientii cu semne si simptome de diseminare generala trebuie tratati cu Izoniazida, Rimfapicina si Pirazinamida (1200 mg/zi) sau Etambutol (1200 mg/zi). Adaugarea la tratament a Cicloserinei (500 mg x 2/zi) sau a Prednisolonului (40 mg/zi) este utilizata de unele protocoale.[78,74,72].
2. INTRODUCERE
BCG este un agent imunomodulator utilizat in tratamentul tumorilor vezicale superficiale. Se administreaza in urmatoarele situatii:
- profilactic impotriva recidivelor si progresiei dupa indepartarea tumorii;
- tratamentul Cis;
- terapia ablativa a bolii reziduale sau multifocale.
Cele mai multe tulpini de BCG utilizate in tratamentul instilational intravezical al tumorilor vezicale superficale sunt derivate din tulpina Pasteur dezvoltata de Albert Calmette si Camille Guerin in ultima decada a secolului al XIX lea.[74].
Desi toate tulpinile ar trebui sa actioneze similar, in realitate exista diferente intre proprietatile diverselor vaccinuri disponibile. Aceste proprietati, fie ca sunt de natura fizica, fie de natura biologica, pot diferi ca nivel de eficacitate.
Exista studii comparative intre tulpinile de BCG, care au aratat ca imunogenitatea unui preparat este legata direct de viabilitatea vaccinului respectiv, de abilitatea bacililor de a se multiplica in vivo si de numarul de unitati formatoare de colonii (CFU) per flacon, respective per instilatie.[74].
Tumorile vezicale superficiale si, mai ales, carcinomul in situ (Cis), au din anul 1976 un nou tratament profilactic eficient, imunoterapia intravezicala nespecifica cu BCG.
Cis, cel mai superficial cancer vezical, cu o puternica tendinta la invazie, beneficiaza azi, probabil, cel mai eficient de terapia intravezicala cu BCG.
Este demonstrat ca exista modificari histologice concomitente ale mucoasei vezicale prezente in 60 - 80% din cazuri, in 10% din cazuri este pus in evidenta faptul ca Cis sunt asociate tumorilor vezicale superficiale.[72,75].
MATERIAL SI METODA
In perioada 2002-2008 s-au internat
in Clinica de Urologie a Spitalului Clinic Judetean de Urgenta
3.1 STRUCTURA PE SEXE A PACIENTILOR
Din cei 204 pacienti cu diagnosticul de tumora vezicala superficiala, 59% au fost barbati (120 pacienti) si 41% au fost femei (84 pacienti).
|
Sex |
Numar pacient |
Procent |
|
Barbati |
120 |
59% |
|
Femei |
84 |
41% |
|
TOTAL |
204 |
100% |
Tabel nr.1
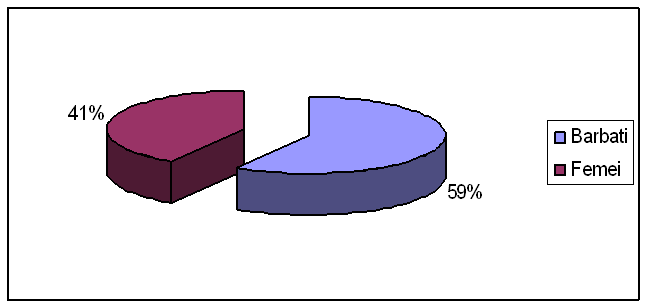
Grafic nr.2 Reprezentarea grafica a repartitiei pe sexe a pacientilor
Din totalul de pacienti, 204, 63% (128 pacienti) au avut varste cuprinse intre 45-60 ani iar restul de 37% (76 pacienti) varste cuprinse intre 60-83 ani.
|
Varsta pacientilor |
Numar pacienti |
Procent |
|
Intre 45-60 ani |
128 |
63% |
|
Intre 60-83 ani |
76 |
37% |
Tabel nr.3 Varsta pacientilor
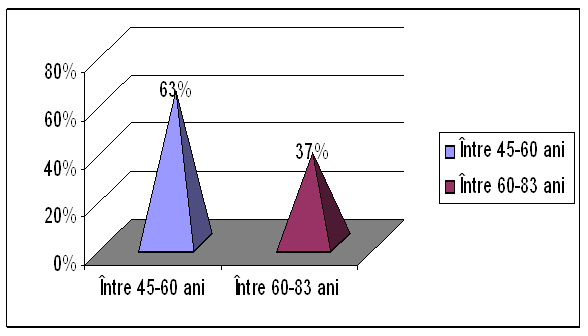
Grafic nr. 4
Dintre pacientii cu varste cuprinse intre 45-60 ani, respectiv 128 pacienti, 73% (93 pacienti) au fost de sex masculin si 27% (35 pacienti) de sex feminin.
|
Sexul pacientilor |
Numar pacienti |
Procent |
|
Masculin |
93 |
73% |
|
Feminin |
35 |
27% |
Tabel nr.5
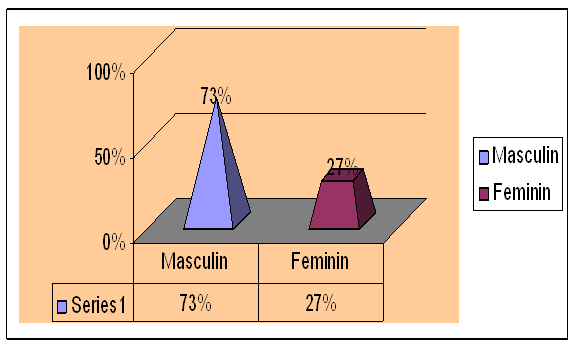
Grafic nr.6
Dintre pacientii cu varste cuprinse intre 60-83 ani, respective 76 pacienti, 51% (39 pacienti) au fost de sex masculin, iar 49% (37 pacienti) au fost de sex feminin.
|
Sexul pacientilor |
Numar pacienti |
Procent |
|
Masculin |
39 |
51% |
|
Feminin |
37 |
49% |
Tabel nr.7
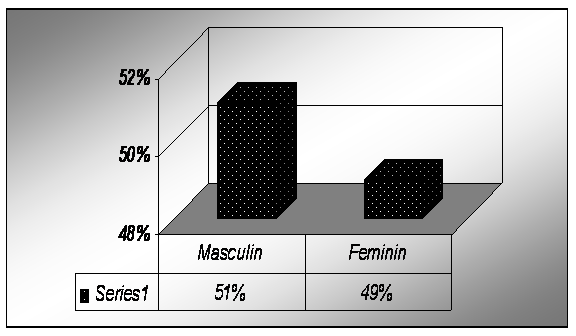
Grafic nr. 8
3.2 STRUCTURA IN FUNCTIE DE MEDIUL DE PROVENIENTA
Incidenta tumorilor vezicale superficiale difera in functie de mediul de provenienta al pacientului. Astfel marea majoritate a pacientilor luati in studiu au provenit din mediul rural, 61% (125 pacienti), iar restul de 39% (79 pacienti), au provenit din mediul urban. Acesta discordanta se poate datora in special faptului ca pacientii din mediul rural au mai putine posibilitati de investigare uzuala si examinari paraclinice, dar mai ales ca delasarea este unul din cele mai importante " calitatii" ale pacientului suferind de orice maladie. I n concluzie, cu cat de intarzie si amana prezentarea pacientului la medicul de familie si respectiv medicul urolog, cu atat mai mult scad sansele unei vindecari mai rapide si cu minimum de suferinta.
|
MEDIUL DE PROVENIENTA |
NUMAR PACIENT |
PROCENT |
|
RURAL |
125 |
61% |
|
URBAN |
79 |
39% |
|
TOTAL |
204 |
100% |
Tabel nr.9
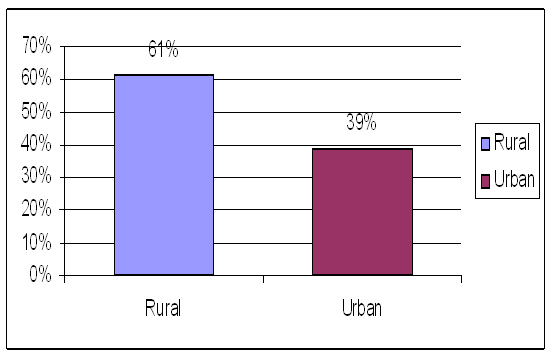
Grafic nr. 10 Reprezentarea grafica a mediului de provenienta
3.3 MODALITATEA DE DEBUT
Debutul in tumorile vezicale superficiale poate fi acompaniat de semne si simptome clinice care orienteaza medicul spre diagnosticul corect sau uneori poate fi insidios si chiar asimptomatic. Majoritatea pacientilor internati au prezentat hematurie 76% (155 pacienti), un numar important au prezentat polakiurie 17% (35 pacienti), un numar mai mic disurie, 4% (8 pacienti), iar un numar si mai mic de pacienti cu tumori vezicale superficiale au fost descoperiti intamplator in urma unor investigatii de rutina, fiind asimptomatici, 3% (6 pacienti).
|
Modalitatea de debut |
Numar pacienti |
Procent |
|
Hematurie |
155 |
76% |
|
Polakiurie |
35 |
17% |
|
Disurie |
8 |
4% |
|
Asimptomatic |
6 |
3% |
Tabel nr.11
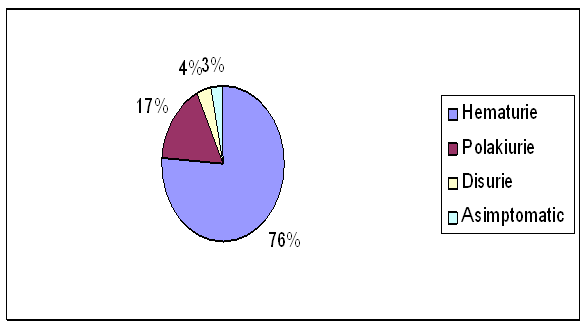
Grafic nr.12 Modalitatea de debut in TVS
3.4 PROTOCOLUL DE DIAGNOSTIC
Acesta cuprinde mai multe etape:
a) Etapa clinica: 1.Anamneza
2. Examenul obiectiv local si general
b) Etapa examinarilor de laborator: 1. a )uzuale - hematologice, hepatice, metabolice.
b) specifice - citologia urinara exfoliativa.
2. teste antigenice (testul BTA)
c) Etapa examinarilor paraclinice: 1. ecografia
2. urografia
3. cistoscopia cu biopsia mucoasei pentru examen
histologic.
|
Investigatii |
Numar pacienti |
Procent |
|
Examen obiectiv local |
204 |
100% |
|
Ecografie |
123 |
60% |
|
UIV |
54 |
27% |
|
Cistoscopie |
204 |
100% |
|
Biopsie |
190 |
93% |
Tabel nr. 13
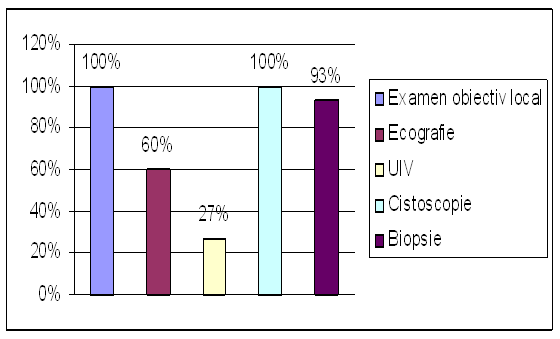 Grafic nr.15
Grafic nr.15
LOCALIZAREA TUMORILOR
Diversitatea localizarii tumorilor vezicale superficiale se datoreaza faptului ca acestea pot da extensii la orificiile ureterale, unilateral sau bilateral (foarte rar, dar posibil) si extensii la nivelul colului vezical.
Cea mai frecventa localizare este la nivelul trigonului, 50% (102 pacienti), din acestia 29% (58 pacienti) au prezentat tumori limitate la trigon, 12% (25 pacienti) au prezentat tumori cu extensie la orificiile ureterale [10% (21 pacienti) extensie unilaterala, iar 2% (4 pacienti), extensie bilaterala], iar restul de 9% (18 pacienti), din cei 50%, au prezentat extensie la colul vezical.
Un numar important de pacienti au localizarea tumorii in peretii laterali ai vezicii urinare, 24% (50 pacienti), din care la 18% (37 pacienti) s-au descoperit tumori unilateral, iar la 6% (13 pacienti) s-au evidentiat tumori bilateral.
Alte localizari deosebite ale tumorilor vezicale superficiale sunt pe peretele anterior, evidentiate la 21% (42 pacienti) si in domul vezical la 5% (11 pacienti).
|
Localizarea tumorii |
Numar pacient |
Procent |
|
Strict limitata la trigon |
58 |
29% |
|
Trigon+extensie unilaterala la orificiul ureteral |
21 |
10% |
|
Trigon+extensie bilaterala la orificiile ureterale |
4 |
2% |
|
Trigon+ extensie la nivelul colului vezical |
18 |
9% |
|
Tumoare pe peretele lateral-bilaterala |
13 |
6% |
|
Tumoare pe peretele lateral-unilaterala |
37 |
18% |
|
Tumoare pe peretele anterior |
42 |
21% |
|
Tumoare in domul vezical |
11 |
5% |
Tabel nr.16
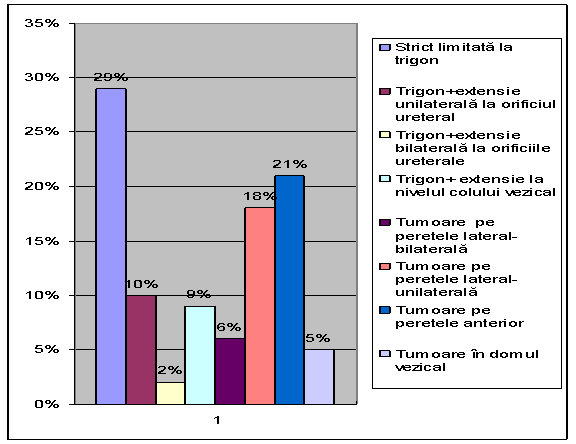
Grafic nr.17 Reprezentarea grafica a localizarii tumorilor
Fig.nr.18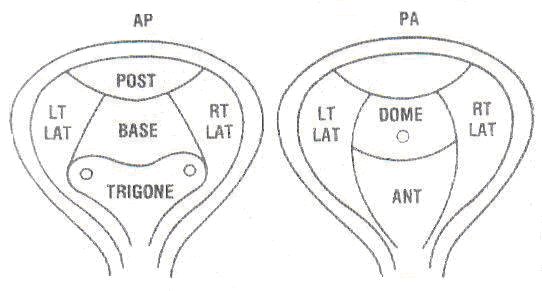
Topografia vezicii urinare [52].
NUMARUL TUMORILOR
Tumora vezicala poate fi unica sau multipla. Aceasta se poate determina prin investigatii. In urma acestora, in cadrul studiului nostru s-a demonstrat urmatoarele:
b) la 32% (65 pacienti) s-a gasit o singura tumora;
c) la 40% (80 pacienti) s-au gasit cate doua tumori;
d) la 28% (59 pacienti) s-au gasit cate trei tumori concomitent.
|
NUMAR TUMORI |
NUMAR PACIENT |
PROCENT |
|
O tumora |
65 |
32% |
|
Doua tumori |
80 |
40% |
|
Trei tumori |
59 |
28% |
|
TOTAL |
204 |
100% |
Tabel nr.19
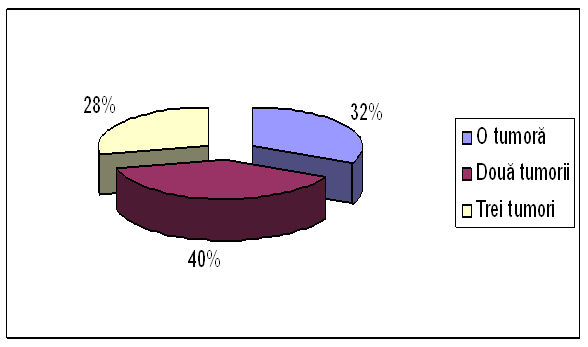
Grafic nr.20 Numarul de tumori concomitente
DIMENSIUNILE TUMORILOR
Dimensiunile tumorilor luate in studiu nostru variaza de la tumori cu dimensiuni < 1cm pana la tumori cu dimensiuni de 2-3 cm (unele cazuri de tumori chiar de peste 3 cm).
Astfel s-au evidentiat 46% (93 pacienti) cu tumori < 1cm, 38% (79 pacienti) cu tumori ce au dimensiunea intre 1-2 cm, iar cele mai putine cazuri au fost cu tumori ce aveau dimensiunea intre 2-3 cm,16%( 32 pacienti).
|
Dimensiunea tumorii |
Numar cazuri |
Procent |
|
<1 cm |
93 |
46% |
|
1-2 cm |
79 |
38% |
|
2-3 cm |
32 |
16% |
|
Total |
204 |
100% |
Tabel nr. 21
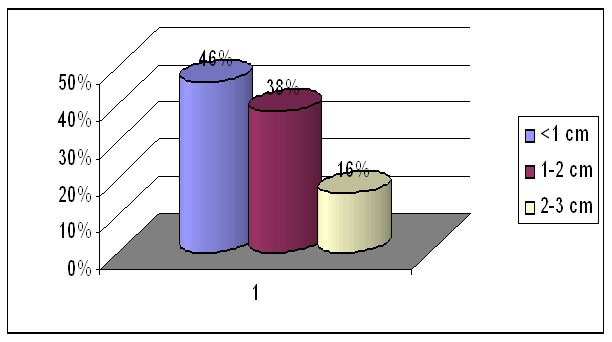
Grafic nr.22 Dimensiunile tumorilor
GRADINGUL TUMORAL
Gradingul tumoral se obtine din examenul anatomo-patologic al produselor de biopsie. In urma acestui procedeu s-au gasit urmatoarele:
a) 76% ( 155 pacienti) prezentau G1;
b) 18% ( 37 pacienti) prezentau G2;
c) 6% ( 12 pacienti) prezentau G3.
|
Grading tumoral |
Numar cazuri |
Procent |
|
G1 |
155 |
76% |
|
G2 |
37 |
18% |
|
G3 |
12 |
6% |
|
Total |
204 |
100% |
Tabel nr.23
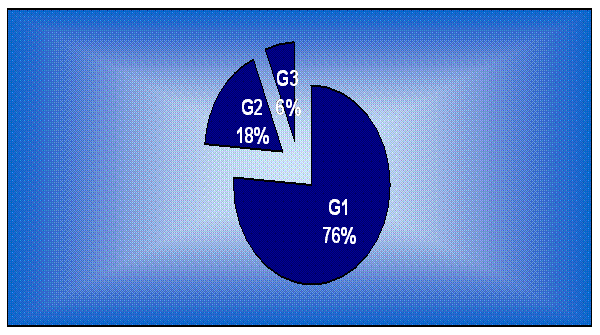
Grafic nr.24 Gradingul tumoral
PROTOCOLUL DE URMARIRE
Tratamentul care a fost aplicat in cazul tuturor pacientilor a fost TUR-V, apoi s-a efectuat examen histopatologic care a evidentiat gradingul tumoral.
Tratamentul instilational cu BCG s-a inceput la o luna de la TUR-V, cu doza de 150 mg (100 ml), o data pe saptamana timp de 6 saptamani iar apoi o data timp de 6 luni.
Pacientii au fost examinati paraclinic la 3 luni, 6 luni si 2 ani postoperator. Astfel s-au gasit urmatoarele:
La 3 luni postoperator:
Ecografia- nu gaseste nimic patologic.
Cistoscopia- 96% (195 pacienti) rezultat To
4% (9 pacienti) recidiva locala, se efectueaza din nou TUR-V.
Probe functionale renale- normale.
|
Rezultat cistoscopie |
Numar pacienti |
Procent |
|
To |
195 |
96% |
|
Recidiva locala |
9 |
4% |
Tabel nr.25
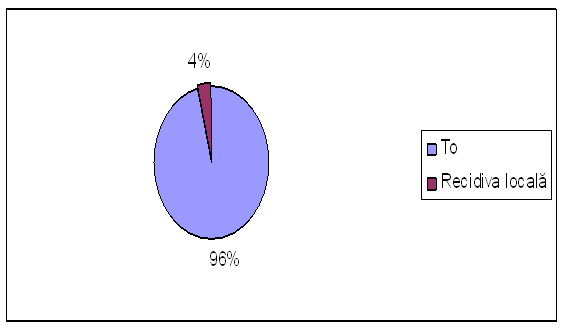
Grafic nr.26 Recidiva locala la 3 luni postoperator
La 6 luni postoperator:
Ecografia- To in toate cazurile.
Cistoscopia- 98% (200 pacienti) rezultat To.
2% ( 4 pacienti) recidiva locala.
|
Rezultat cistoscopie |
Numar pacienti |
Procent |
|
To |
200 |
98% |
|
Recidiva locala |
4 |
2% |
Tabel nr.27
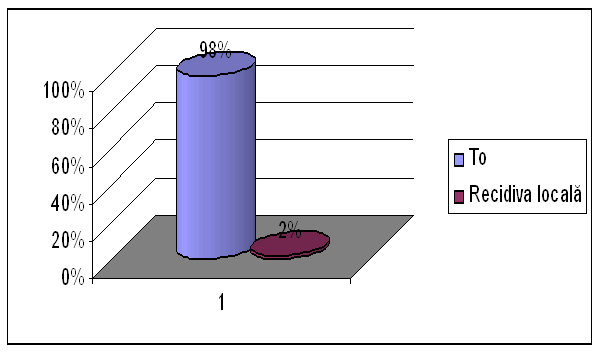
Grafic nr.28 Recidiva locala la 6 luni postoperator
S-a efectuat urocultura la toti pacienti. Rezultatele au fost:
a) 5% (10 pacienti) pozitiva;
b) 95% (194 pacienti) negativa.
In urina pacientilor s-a gasit predominant E. Coli, dar am mai fost gasite si alte bacterii (Enterobacter).
|
Urocultura |
Numar pacienti |
Procent |
|
Pozitiva |
10 |
5% |
|
Negativa |
194 |
95% |
Tabel nr.29
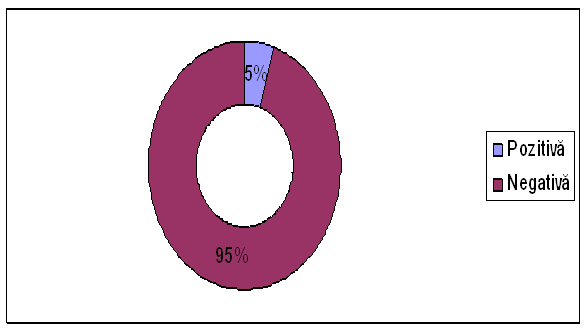
Grafic nr.30 Urocultura la 6 luni postoperator
La 2 ani postoperator:
Cistoscopia- s-au gasit recidive locale astfel:
a) G1= 18 pacienti (11,60%) din 155 pacienti;
b) G2= 6 pacienti (1,60%) din 37 pacienti;
c) G3= 1 pacient (0,08%) din 12 pacienti.
|
Rezultat citoscopie |
Numar pacienti |
Procent |
|
G1 |
155 |
11,60% |
|
G2 |
37 |
1,60% |
|
G3 |
12 |
0,08% |
Tabel nr.31
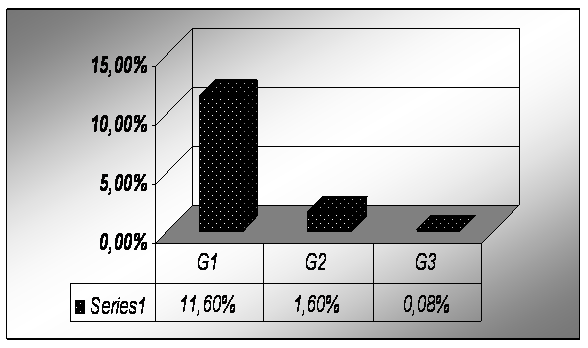
Grafic nr.32
REZULTATE SI DISCUTII
Vaccinul BCG folosit in instilatii vezicale :
stimuleaza formatiuni imunitare nespecifice, care distrug celulele tumorale;
stimuleaza mecanismele imune antitumorale specifice prin reactia incrucisata intre BCG si antigenele tumorale;
produce inflamatii, cu ischemie si distrugerea celulelor tumorale.
Indicatia de tratament instilational intravezical cu BCG in contextul admis actual este:
1. Tumorile pTa recidivate (mai mult de 2 recidive in decurs de 1 an), in special daca sunt rezistente la chimioterapie.
2. Tumori pTa asociate cu alti factori de agravare ca: grading G3, multifocalitate, displazie severa asociata pe o suprafata mai mare de 5 cm.
3. In tumorile pTl terapia BCG este indicata in toate cazurile, cu toate ca unii autori indica utilizarea initiala a chimioterapiei si numai apoi BCG in absenta raspunsului pozitiv.
4. Tratamentul de baza al carcinomului ' in situ' singular sau asociat cu tumori pTa sau pT1.
5. Tratamentul tumorilor reziduale post TUR.V. [72,71,79,80,81,82].
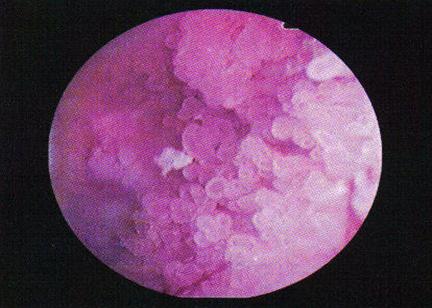
Fig. nr.33 Aspect de tumora vezicala inainte de TUR-V si BCG [61].
4.1 Dozele si calea de administrare a BCG-ului
Schemele optime ale tratamentului cu BCG inca nu sunt determinate. Morales a propus folosirea a 120 mg BCG diluat in 50 ml ser fiziologic, instilat in vezica timp de 2 ore. Concomitent se administreaza 5 mg vaccin intradermic .
Dozele propuse pentru utilizare
variaza de la 75 Ia 150 ml si depind de tipul vaccinului folosit (Pasteur,
Tice, Glaxo,
Calea de administrare
1. Injectarea intravezicala, la baza tumorii - s-a raportat in 1975 si a fost propusa de Martinez Pineiro si Muntanola.
2. Administrarea prin scarificare cutanata - a fost propusa fie singura, fie combinata cu injectii in leziune, de aceiasi autori.
3. Instilatii intravezicale combinate cu administrare prin scarificare - propusa de A. Morales si colaboratorii sai in 1976.
4. Administrare orala - propusa de Netto si Lemos in 1983.[70,72,75].
Injectiile intralezionale au fost rapid abandonate, datorita efectelor adverse severe.
Administrarea orala s-a dovedit a fi clar inferioara instilatiilor intravezicale si niciodata nu a castigat adepti.
BCG administrat numai prin scarificare a dovedit eficienta impotriva aparitiei metastazelor, desi a fost dificil de estimat valoarea reala, dar nu a avut eficacitate antitumorala ablativa. Din aceste cauze, calea de administrare a BCG in tumorile vezicale superficiale unanim acceptata este calea intravezicala.[70,72,75].
Tratamentul intravezical pentru imuno-profilaxia si ablatia cancerului restant vezical superficial, indeplineste cele patru cerinte de eficienta optima a BCG si anume:
1. contactul direct dintre BCG si celulele tumorale;
2. masa tumorala trebuie sa fie mica;
3. doza trebuie sa fie adecvata, si
4. tumorile raspund mai bine la tratament cand sunt limitate la organul din care s-au dezvoltat.[70,72,75].
Limitele terapiei instilationale intravezicale cu BCG sunt date de pacientii cu tumori cu risc scazut sau intermediar la care chimioterapia intravezicala este prima alegere.
Terapia este contraindicata la pacientii cu cancer vezical T2 sau mai mare (unde indicatia este de cistectomie), la imunocompromisi (HIV, sindrom de imunodeficienta congenitala sau pacienti cu tratament imunosupresiv), pacienti cu alte carcinoame progresive (leucemie, boala Hodgkin), pacienti cu tuberculoza activa, gravide, femei care alapteaza.[72,75].
4.2 Eficacitatea tratamentului cu BCG
Studiile comparative ale BCG cu citostaticele intravezicale au aratat superioritatea neta a BCG in fata Thyotepa, Mitomycin sau Doxorubicin.[77,78,81,88,89].
4.3 Eficienta pe termen lung a BCG-ului
Obiectivul pe termen lung al oricarui tratament adjuvant pentru tumori vezicale superficiale ste sa previna progresia bolii si sa inbunatateasca supravietuirea. Desi chimioterapia intravezicala a redus rata de recidiva tumorala pe termen scurt, aceasta nu a atins acelasi obiectiv pe termen lung, si anume acela de prevenire a progresiei bolii.[37,38,75,90].
4.3 Schemele terapeutice
Schemele terapeutice variaza foarte mult de la cure scurte de 6-12 saptamani pana la cure de intretinere, pe o perioada de 2-3 ani.
Toti clinicienii sunt de acord ca instilatiile intravezicale cu BCG nu trebuie incepute mai devreme de 3 saptamani de la TUR-V, pe o mucoasa inca necicatrizata, deoarece exista risc de diseminare sistemica bacilara.[59,75,76,85,86,87].
De asemenea, majoritatea clinicieniilor sunt de accord ca obtinerea inductiei unui raspuns imun bun calitativ si de durata se obtine, posibil dupa 4 saptamani, dar cu certitudine dupa 6 saptamani de la inceperea terapiei intravezicale cu BCG.[70,86,87]. Sunt si unii clinicieni care accepta idea curelor lunare de intretinere, pe o perioada de timp variabila (4-12 luni).[75,85,86,87,91].
Cea mai moderna schema terapeutica ramane urmatoarea:
dupa TUR-V se aplica instilatii saptamanale timp de 6 luni (inductie);
urmate de 6 instilatii lunare;
apoi o instilatie din 3 in 3 luni timp de inca un an si jumatate.[70].
Zlotta si colaboratorii sai au fost cei care au observat ca raspunsul imun limfoproliferativ atinge maximum la 4 saptamani de la inceperea instilatiilor cu BCG in 80% din cazuri, ajunge la 100% dupa 5 saptamani de cura si revine la valorile preterapeutice dupa 6 luni de la incheierea acesteia.[87].
Intr-un studiu efectuat de Southwest Oncology Group (SWOG) in 2000 de Lamm s-a demonstrate ca pacientii care au primit 6 saptamani terapie de inducere cu BCG si apoi 3 saptamani consecutive 3 luni, 6 luni si apoi la fiecare 6 luni timp de 3 ani au avut o rata de recidiva semnificativ mai buna, recidivele la 7 ani scazand de la 52% la 25% decat pacientii care au beneficiat doar de primele 6 saptamani de inducere. Beneficiul substantial a fost in mod evident pentru pacientii cu tumori superficiale care nu aveau si carcinom in situ. [84].
Terapia BCG, are multe aspecte care nu sunt inca elucidate si necesita studii aprofundate pentru obtinerea raspunsului. Aceste aspecte sunt:
Nu sunt clare mecanismele efectoare ale BCG.
Nu au fost identificate cele mai bune tulpini si dozele optime.
Nu este studiat efectul combinat al BCG cu alti imunomodulatori.
Desi BCG este mai eficace in comparatie cu chimioterapia, toxicitatea sa este semnificativ crescuta. Sunt necesare studii in vederea diminuarii ei. [72,75].
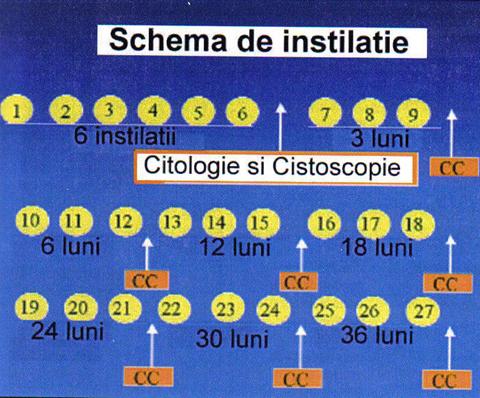
Fig.nr. 34 Schema Lamm pentru instilatiile cu BCG [84].
4.5 Complicatiile tratamentului cu BCG
Aplicarea BCG intravezical pentru cancer vezical superficial este mai toxica decat chimioterapia.
Au fost descries: - complicatii locale,
- complicatii sistemice severe,
- infectii septice fatale .
Severitatea efectelor adverse locale sau sistemice este apreciata in mod diferit de diversi urologi. Astfel, unii sisteaza tratamentul BCG la aparitia cistitei sau a febrei, in timp ce altii, considera ca efectele BCG se manifesta numai in acest caz si nu le vor considera ca efecte adverse.[92].
BCG induce mai multe efecte adverse decat Mitomycina, atat local cat si sistemic. Instilatiile vezicale cu BCG pot induce infectii urinare banale la un numar considerabil de pacienti.
Febra, apare la 4-6 ore dupa instilatie, are de obicei un caracter sporadic si nu necesita tratament specific. Febra care se mentine peste 2 zile, indica o stare mai alarmanta, si impune initierea tratamentului cu Izoniazida (350 mg/zi), Etambutol (2OOmg/zi) si Rifampicina (6OOmg/zi), care se mentine timp de 3 luni. La barbati, in unele cazuri, poate sa apara prostatita, care nu necesita tratament specific.
Alte complicatii: hematurii intermitente, febra pasagera , pielocistite, stricturi uretrale, tulburari digestive, prostatite granulomatoase, stenoze de meat uretral, obstructii uretrale, supuratii peno-scrotale, retentii acute de urina, artrite etc.[92].

Fig. nr. 35 Aspect endoscopic al Cis cu hematurie dupa instilatii cu BCG [61].
Referitor la lotul nostru de studiu, complicatiile au fost indeosebi medii, acestea au remis la cateva zile dupa tratament simptomatic.
Dintre reactiile adverse descriem aparitia semnelor locale si generale.
Semnele locale sunt reprezentate de cistita, 88% (180 pacienti) si un numar mai redus de pacienti care au prezentat hematurie, 38% (79 pacienti), dureri suprapubiene izolate sau perianale 55% (112 pacienti).
Semnele generale sunt reprezentate de febra, 82% (167 pacienti), artrita 52% (106 pacienti) si in cel mai rau caz, s-au prezentat pacienti cu detresa respiratorie, colaps cardio-vascular, hepatita, septicemia, 1% (21 pacienti cu septicemie) care poate fi fatala.
|
Semne locale |
Numar pacienti |
Procent |
|
Cistita |
180 |
88% |
|
Hematurie |
79 |
38% |
|
Dureri suprapubiene izolate |
112 |
55% |
Tabel nr.36

Grafic nr. 37 Semnele locale dupa tratamentul cu BCG
|
Semne generale |
Numar pacienti |
Procent |
|
Febra |
167 |
82% |
|
Artrita |
106 |
52% |
|
Septicemia |
21 |
1% |
Tabel nr.38

Grafic nr.39 Semnele generale dupa tratamentul cu BCG
CONCLUZII
1. Imunoterapia intravezicala cu BCG s-a dovedit a fi utila pentru profilaxia recidivelor tumorilor vezicale superficiale.
2. Majoritatea pacientilor diagnosticati cu tumoare vezicala superficiala sunt de sex masculin ( 59% ), frecventa maxima de aparitie fiind la varsta de 62 ani.
3. Cea mai frecventa forma de debut este reprezentata de hematuria, 76%, oricarui bolnav cu hematurie trebuie sa i se efectueze cistoscopie in anestezie, in conditii de spitalizare.
4.Hematuria macroscopica este motiv pentru care pacientii trebuie sa se prezinte la medicul de familie, si respectiv medical urolog, in vederea efectuarii examinarilor paraclinice , care sa lamureasca cauza hematuriei.
5.Ignoranta bolnavului fata de simptomele aparute sau faptul ca simptomele nu-i trezesc banuieli bolnavului, fac ca bolnavul sa se prezinte la medic in stadii destul de avansate sau chiar terminale (stadiul T3 si T4).
6. Majoritatea pacientilor sunt din mediul rural 61% , aceasta datorandu-se in mare parte adresabilitatii intarziate a pacientilor.
7. In cadrul protocolului de diagnostic al unei tumori vezicale superficiale, la un pacient cu simptomatologie sugestiva, principalele metode sunt reprezentate de tuseul rectal cu palpare bimanuala a hipogastrului sub anestezie cu miorelaxare, efectuat la toti pacientii lotului studiat si de cistoscopie cu o reusita in diagnostic de 100%, ambele impunandu-se cu caracter obligatoriu la orice pacient.
8. Pentru diagnostic complet si de certitudine este esentiala efectuarea cistoscopiei cu prelevare bioptica a unor fragmente de mucoasa vezicala in scopul examinarii histopatologice.
9. Pentru certitudinea diagnosticului se efectueaza biopsia la 93% pacienti.
10. Pentru diagnosticul precoce al tumorilor vezicale superficiale si mai ales a carcinomului in situ, se foloseste citologia exfoliativa si determinarile cu anticorpi monoclonali ( BTA-test ).
11. Localizarea tumorilor este preponderent limitata la trigon, 29%, tumori pe peretele anterior, 21%, iar tumorile cele mai putine au fost acelea care ating trigon si dau extensie bilaterala la orificiile ureterale, 2%.
12. S-au evidentiat 40% pacienti cu cate doua tumori concomitente si 28% pacienti cu cate trei tumori concomitnte.
10. Majoritatea tumorilor studiate au avut dimensiuni sub 1 cm, 46%, dimensiunea mica este un avantaj, permitand o abordare chirurgicala mai usoara si vindecare mai rapida.
13. Potrivit studiului efectuat, s-au gasit 6% tumori cu grading G3 si 76% tumori cu grading G1.
14. Pentru scaderea numarului de recidive tumorale se recomanda efectuarea unei rezectii transuretrale per primam (TUR-V), urmata de terapia adjuvanta cu instilatii intravezicale cu BCG obtinand astfel o eficacitate crescuta a tratamentului si asigurand o calitate satisfacatoare vietii ulterioare a pacientului.
15. Tratamentul instilational cu BCG nu trebuie inceput mai devreme de 3 saptamani de la TUR-V, pe o mucoasa inca necicatrizata, deoarece exista risc de diseminare sistemica bacilara.
16. Cea mai moderna schema terapeutica ramane urmatoarea:
dupa TUR-V se aplica instilatii saptamanale timp de 6 luni (inductie);
urmate de 6 instilatii lunare;
apoi o instilatie din 3 in 3 luni timp de inca un an si jumatate.
17. Tratamentul instilational cu BCG are la baza mecanismele proprii de aparare ale organismului si constituie o metoda eficienta in consolidarea terapiei chirurgicale a tumorilor vezicale superficiale permitand ameliorarea semnificativa a ratei supravietuirii si chiar vindecarea.
18. Dupa tratament se urmareste aparitia recidivelor, efectuandu-se controlul cistoscopic efectuat obligatoriu sub rahianestezie la interval de 3 luni in primul an, apoi la 6 luni in al 2- lea an si anul ulterior, alaturi de examinarile de laborator.
19. Pentru o identificare histologica corecta trebuie rezecat tesut pentru biopsie la 5 mm de marginile tumorii din 4 puncte la orele 3, 6, 9, 12 ( biopsie marginala in cadrane ) sau, pentru orice situatie in care se suspecteaza o recidiva se vor recolta biopsii tintite si randomizate ( cardinale si din patul tumoral ), iar daca se confirma recurenta tumorala aceasta se va rezolva dupa acelasi protocol terapeutic.
20. Rezultate bune la 2 ani postoperator, s-au gasit recidiva locale la 18 pacienti din 155, cu grading G1, si la 1 pacient din 12, cu grading G3.
21. Valoarea tratamentului instilational intravezical cu BCG este net superioara altor tipuri de tratamente ( Thyotepa, Doxorubicin, Mitomycin) in cazul tumorilor vezicale superficiale.
BIBLIOGRAFIE
1.
32. Sanclemente G, Gill DK - Human papillomavirus molecular biology and pathogenesis. J Eur Acad Dermatol Venereol 2001;16:231-40. 33. Jones PA, Droller MJ - Bazele moleculare ale dezvoltarii tumorlor vezicii urinare. Semin Urol, 2003;11:177-192. 34. Brandan S, Bohle A - Bladder cancer. Molecular and genetic basis of carcinogenesis. Eur Urol 2001;39:491-497. 35. Murphy WM, Soloway MS - Urothelial displasia. J Urol 2003;127:849. 36. Kurth KH - Diagnosis and treatment of superficial transitional cell carcinoma of the bladder: Facts and perspectives. Eur Urol 2001;31 (suppl 1):10-19. 37. Ibrahim E, Ghoneim M,Nigam V, Brailovsky C - Prophylactic maltose tetrapalmintate and BCG immunotherapy of recurent superficial bladder tumors. Preliminary report. The J Urol 2003;140:498-506. 38. Kurth KH, Bouffioux C, Sylvester R, van der Meiden APM, Oosterlinck W, Brausi M and members of the EORTC GU Group - Treatment of superficial bladder tumors: Achievements and needs. Eur Urol 2000;37 (suppl 3):1. 39. Epstein JI, Amin MB, Reuter VR, Mostofi FK - The World Health Organization/International Society of Urological Pathology consensus classification of urothelial (transitional cell) neoplasms of urinary bladder. Bladder Consensus Conference Committee. Am J Surg Pathol 2000;22(12):1435-48. 40. Fujii Y, Fukui I, Kihara K, Tsujii T, Kageyama Y, Oshima H - Late reccurence and progression after a long tumor-free period in primary Ta and T1 bladder cancer. Eur Urol 2000;36:309-313. 41. Kausch I, Bohle A - Bladder cancer. Molecular aspects and diagnosis. Eur Urol 2001;39:498-506. 42.Sachs M, Schlechte H, Leak V - Genetic analysis of Tp53 from urine sediment as a tool for diagnosis reccurence and residual of bladder carcinoma. Eur Urol 2000;38:426-433. 43. Kroft SH, Oyasu R - Urinary bladder cancer: Mechanism of development and progresion. Lab Invest 2004;71:158-174. 44. Flanigan R, Ellison M, Butler K - A trial of prophylactic thiotepa or mitomycim C intravesical therapy in patients with reccurent or multiple superficial bladder cancers. The J Urol 2001;136:35-40. 45. Bono AV, Hall RR, Denis L, Lovisto JA, Sylvester R and members of EORTC Genito-Urinary Group - Chemoresection in Ta bladder cancer. Eur Urol 2001;29:385-390. 46. Coppin C, Gospodarowicz M - The NCI Canada trial of concurent cisplastin and radiotherapy for muscle invasive bladder cancer. J Clin Oncol 2000;14:2901-2907. 47. Hamden P, Eardley I, Joyce AD, Southgate I - Cytokeratin 20 as an objective marker of urothelial dysplasia. Br J Urol 2001;78:870-878. 48. Gluck G, Ardelean C, Hortopan M, Mihai M,Costache B, Sabau V, Sinescu I - Valoarea prognostica a markerului Ki 67 pentru tumorile vezicale Al XXI-lea Congres National de Urologie.2003. 49. Conferinta de Consens asupra neoplasmelor uroteliale organizata de OMS si ISUP (International Society of Urological Pathology) - clasificarea TV.2004. 50. Amin MB, McKenney JK - An approach to the key diagnosis of flat intraepithelial lesions of the urinary bladder using the World Health Organization/International Society of Urology Pathology consensus classification system. Adv Anat Pathol 2002;9:222-232. 51. Sinescu I - Urologie clinica, Ed. Medicala Bucuresti Amaltea 1999. 52. Moga AS - Curs de Oncologie, Partea speciala pentru studenti, Ed. Alma Mater, Sibiu,2006; 221-225. 53. Wallace DM - Tumors of the Bladder, Ed. Livingstone. Editia a XV-a, 2001. 54. Vallancien G, Veillon B, Charton M, Brisset J - Can transabdominal ultrasonography of the bladder replace cystoscopy in the follow-up of superficial bladder cancer tumors? The J Urol 2001;136:32-37. 55. Proca E - Tumorile vezicii urinare. Tratat de patologie chirurgicala (sub redactia). Ed. Med 2000;2:182-232. 56. Fontaniere B, Ranchere-Vince D, Landry JL et col. - Criteres de qualite de la cytologie urinaire pour le diagnostic tumoral. In "Progres en urology",2001;11,nr.5:867-875. 57. Gluck G, Gluck M - Hematurie de cauza rara: sterilet migrat in vezica urinara. Revista Romana de Urologie, vol 4, 2005,nr.1, pag.41-43. 58. Revista Romana de Urologie, vol V, nr.3-4, 1999, pag.211. 59. Oosterlinck W, Lobel B, Jakse G, Malmstrom P, Stockle M, Stemberg C - Guidelines on bladder cancer. Eur Urol 2002;41:105-112. 60. Nicolescu D - Bazele chirurgiei endourologice, Ed. Eurobit 2000. 61. Geavlete P - Atlas of endourology.. 62. Amling CK, Trasher GB, Frazier H, Hodge RK, Paulson DF - Radical cystectomy for stage Ta,Tis and T1. TCC of the bladder, J Urol, 2002;151:31-36. 63. Gattegno B, Chopin D - Progres en Urologie (2001), 11, nr.5, 963-990. 64. Freeman JA, Skinner DC - Radical Cystectomy for high risk patients with superficial bladder cancer in the era of orthotopic urinary reconstruction. Cancer 2000;75:33-39. 65. Stockle M, Meyerburg W, Wellek S - Adjuvant polychemotherapy of non-organ confined bladder cancer after radical cystectomy revisited: Long term results of a controlled prospective study and further clinical experince. J Urol 2001;153:47. 66. Malkowicz Sb, Nichols P, Lieskovsky G, Boyd SD, Huffman J, Skinner DG - The role of radical cystectomy in the management of high grade superficial bladder cancer (PA, P1, PIS and P2). J Urol 2001;144(3):p.641-5. 67. Pauwels R, Scharpes RF, Smeets AW, Debruyne FM, Geraedts JP - Grading in superficial bladder cancer. (1). Morphological criteria. Br J Urol, 2003. 61(2):p.129-34. 68. Wishnow KI, Dmochowski R - Pelvic reccurence after radical cystecomy without peroperative radiation. J Urol 2000;33:358. 69. Soloway M - Overview of treatment of superficial bladder cancer. The J Urol 2001;136:539-545. 70. Martinez-Pincero JA, Martinez-Pincero L - BCG update: Intravesical therapy. Eur Urol 2001;31 (suppl 1):31-41. 71. Americam Cancer Society: What are the key statistics on bladder cancer. Internet Reference 2000. 72. Bohle A - for the EBIN Group - BCG's mechanism of action - increasing our understanding. Eur Urol 2000;37 (suppl 1):1-8. 73. Fray F, Marshall N, Brent F, Treiger G - Radical Cystectomy (Anterior Exenteration) in the Female Patients, Urologic Clinics of North America, vol. 18,nr.4. 2001. 74. Muckherjee A, Hart P, Weiss L - Intravesical BCG treatment for superficial bladder cancer; long-term results using two different strains of BCG. Br J Urol 2000;69:147-150. 75. Lamm D - Optimal BCG treatment of superficial bladder cancer as defined by american trials. Eur Urol 2001;21 (suppl 2):12-16. 76. Geavlete P - Imunoterapia cu vaccin BCG in tratamentul profilactic al recidivelor tumorilor vezicale. 2000. 77. Lebret T, Gaudey F, Herve JM, Barre P, Lugange PM, Botto H - Low-dose BCG instillations in the treatment of stage T1 grade 3 bladder tumors: reccurence, progression and success. Eur Urol 2000;34:67-72. 78. Patard JJ, Rodriguez A, Leray E, Rioux-Leclercq N, Guille F, Lobel B - Intravesical bacillus Calmette-Guerin treatment improves patient survival inT1G3 bladder tumors. Eur Urol 2002;41:635-542. 79. Albaga F - Origin of high-grade superficial bladder cancer. Eur Urol, 2002.13 (3):p.153-5. 80. Cole P, Hoover R, Friedell GH - Occupation and cancer of the lower urinary tract. Cancer 2001;29:1250. 81. Farrow GM, Barlebo H, Enjoji M - Transitional cell carcinoma in situ. Progress in clinical and biological research. In: Louis D, Niijima T, Prout G, Schroeder Fh, eds. Developments in bladder cancer. New York: Alan R. Liss, 2001:85-96. 82. Ghoneim M - Orthotopic bladder substitution in women after cystectomy for bladder cancer, BJU, 2004, vol.93.nr.6, pag. 891-908. 83. Heney Nm - Natural history of superficial bladder cancer. Prognostic features and long-term disease course. Urol Clin North Am, 2002. 19 (3):p.429-33. 84. Tanagho EA, Mc Aninch JW - Tumors of the bladder. Gen Urol ed. XII 2000, 355-360. 85. Haaff E, Dresner S, Ratliff T, Catalona W - Two courses of intravesical BCG for transitional cell carcinoma of the bladder. The J Urol 2001;136:820-824. 86. Herr H, Johnson M, Thomas J, Planck M - Superficial bladder cancer trated with BCG: A multivariate analysis of factors affecting tumor progression. The J Urol 2000;141:22-28. 87. Zlotta AR, van Vooren JP, Huyden K, Drowart A, Decock M, Schulman CC - What is the optimal regimen for BCG intravesical therapy? Are six instillations necessary? Eur Urol 2000; 37:470-477. 88.Hurle R, Manzetti A, Micheli E - Tumor progression and survival in patients with T1G3 bladder tumors treated with low-dose Pastuer bacille Calmett-Guerin. Canc det and prev 2000; 24: (suppl 1): 305-307. 89. Thierry L, Gaudez F, Herve Jm, Bane P, Lugagne PH, Botto H - Low-dose BCG instillations in the treatment of stage T1G3 bladder tumors: reccurence, progression and success. Eur Urol 2000;34:67-72. 90. Schellhamer PF, Bean MA, Withmore WF - Prostatic involvement by transitional cell carcinoma: pathogenesis, prognostic. J Urol. 2002;118 (3). 91. Okamura K, Kinukawa T, Tsumua Y, Otani T, Itoh H, Kobayashi M, Mitsuura O, Fukatsu T, Osshima S - A randomized study of short - versus long-term intravesical epirubicin instillation for superficial bladder cancer. Eur Urol 2001;33:285-295. 92. Ramakumar S, Buicyan J, Besse JA, Steven GR, Wollan PC, Blute ML, O'Kane DJ - Comparison of screening methods in the detection of bladder cancer. J Urol 2000; 161:388-394.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 13375
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2026 . All rights reserved